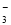题目内容
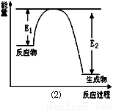
反应 A+B→C(△H<0)分两步进行 ①A+B→X (△H>0)②X→C(△H<0)下列示意图中,能正确表示总反应过程中能量变化的是( )
A.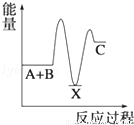 B.
B.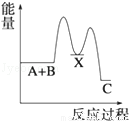 C.
C.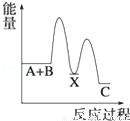 D.
D.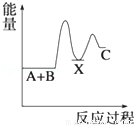
B
【解析】根据物质具有的能量进行计算:△H=E(生成物的总能量)﹣E(反应物的总能量),当反应物的总能量大于生成物的总能量时,反应放热,当反应物的总能量小于生成物的总能量时,反应吸热,以此解答该题.
【解析】
由反应 A+B→C(△H<0)分两步进行 ①A+B→X (△H>0)②X→C(△H<0)可以看出,A+B→C(△H<0)是放热反应,A和B的能量之和大于C,由①A+B→X (△H>0)可知这步反应是吸热反应,X→C(△H<0)是放热反应,故X的能量大于A+B;A+B的能量大于C;X 的能量大于C,图象B符合,
故选B.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目