题目内容
(12分)弱电解质的电离平衡、盐类的水解平衡和难溶物的溶液平衡均属于化学平衡。
I、已知H2A在水中存在以下平衡:H2A H++HA-,HA-
H++HA-,HA- H++A2-。
H++A2-。
⑴NaHA溶液 (选填“显酸性”、 “显碱性”、 “显中性”或“无法确定”)。
⑵某温度下,若向0.1 mol/L的NaHA溶液中逐滴滴加0.1 mol/L KOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是 。
a.c(H+)·c(OH-)=1×10―14 b.c(Na+)+c(K+)=c(HA-)+2c(A2-)
c.c(Na+)>c(K+) d.c(Na+)+c(K+)=0.05 mol/L
⑶已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:
CaA(s) Ca2+(aq)+A2-(aq) △H>0。
Ca2+(aq)+A2-(aq) △H>0。
①温度降低时,Ksp (填“增大”、“减小”或“不变”,下同)。
②滴加少量浓盐酸,c(Ca2+) 。
II、含有Cr2O72-的废水毒性较大,某工厂废水中含5.00×10-3 mol·L-1的Cr2O72-。为使废水能达标排放,作如下处理:
Cr2O72- Cr3+、Fe3+
Cr3+、Fe3+ Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3
⑷欲使10L该废水中的Cr2O72-完全转化为Cr3+,理论上需要加入 g FeSO4·7H2O。
⑸若处理后的废水中残留的c(Fe3+)=2×10-13mol·L-1,则残留的Cr3+的浓度为 。(已知:Ksp[Fe(OH)3]=4.0×10-38 Ksp[Cr(OH)3]=6.0×10-31)
⑴无法确定 ⑵bc ⑶①减小
②增大 ⑷83.4g ⑸3×10-6mol·L-1
【解析】I、(1)NaHA在溶液中既存在水解平衡,又存在电离平衡,水解显碱性,电离显酸性,但水解程度和电离程度哪一个大,却无法判断,所以NaHA溶液的酸碱性无法判断。(2)温度未知,所以c(H+)·c(OH-)的之积不一定是1×10―14。根据电荷守恒可知c(Na+)+c(K+)+c(H+)=c(HA-)+2c(A2-)+c(OH-),溶液显中性,所以选项b一定正确。当二者恰好反应时c(Na+)=c(K+),但此时溶液显碱性,要使溶液显中性,则氢氧化钾的量要少一些,即c(Na+)>c(K+)正确。因为氢氧化钾溶液的体积要小于氢氧化钠溶液的体积,即二者不可能是等体积混合的,所以选项d不正确。(3)因为反应吸热,所以温度降低时,平衡向逆反应方向移动,溶度积常数减小。加入盐酸可以降低A2-的浓度,平衡向正反应方向移动,c(Ca2+)增大。
II、10L该废水中的Cr2O72-的物质的量为5.00×10-3 mol·L-1×10L=0.05mol,得到电子0.05mol×6=0.3mol。根据得失电子守恒可知需要加入FeSO4·7H2O的物质的量为0.3mol,质量是0.3mol×278g/mol=83.4g。根据Ksp[Fe(OH)3]=4.0×10-38和Ksp[Cr(OH)3]可知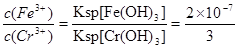 ,所以当c(Fe3+)=2×10-13mol·L-1时,Cr3+的浓度为3×10-6mol·L-1。
,所以当c(Fe3+)=2×10-13mol·L-1时,Cr3+的浓度为3×10-6mol·L-1。

 H++HA-,HA-
H++HA-,HA-
 H++HA-,HA-
H++HA-,HA- Cr3+、Fe3+
Cr3+、Fe3+ Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3