题目内容
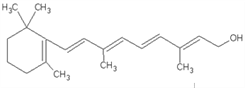
【题目】(1)右图是维生素A的分子结构,维生素A中的含氧官能团是 _________(填名称),维生素A的分子式是 ___________,1mol维生素A最多能与_______mol溴发生加成反应.
(2)在下列物质中是同分异构体的有______________,是同系物的有_____________,属于醇的有____________,核磁共振氢谱吸收峰有4组,且面积比为1:2:2:3的是_____________。
①CH3CH2CH2CH3 ②CH3CH2CH3 ③CH3CH2OH ④CH3COOH ⑤CH3CH2COOH ⑥![]() ⑦
⑦![]() ⑧ CH2=CHCH=CH2 ⑨CH≡CCH2CH3
⑧ CH2=CHCH=CH2 ⑨CH≡CCH2CH3
【答案】 羟基 C20H30O 5 ⑥⑦、⑧⑨ ①②、④⑤ ③⑥ ⑦
【解析】⑴. 根据维生素A的结构可以看出,维生素A中的含氧官能团为羟基,分子式为C20H30O,碳碳双键可以和溴发生加成反应,1mol维生素A中含有碳碳双键5mol,所以1mol维生素A最多能与5mol溴发生加成反应,故答案为:羟基;C20H30O;5;
⑵. 分子式相同、结构不同的有机物互为同分异构体,⑥![]() 的分子式为C7H8O,⑦
的分子式为C7H8O,⑦![]() 的分子式也为C7H8O,二者分子式相同而结构不同,互为同分异构体,⑧ CH2=CHCH=CH2的分子式为C4H6,⑨CH≡CCH2CH3的分子式也为C4H6,二者分子式相同而结构不同,互为同分异构体;结构相似、分子组成相差一个或多个CH2基团的有机物互为同系物,①CH3CH2CH2CH3为烷烃,分子式为C4H10,②CH3CH2CH3也是烷烃,分子式为C3H8,二者结构相似、组成相差一个CH2,所以①②互为同系物,④CH3COOH是一元羧酸,分子式为C2H4O2,⑤CH3CH2COOH是一元羧酸,分子式为C3H6O2,二者结构相似、组成相差一个CH2,所以④⑤互为同系物;分子中含有醇羟基的为醇,③CH3CH2OH和⑥
的分子式也为C7H8O,二者分子式相同而结构不同,互为同分异构体,⑧ CH2=CHCH=CH2的分子式为C4H6,⑨CH≡CCH2CH3的分子式也为C4H6,二者分子式相同而结构不同,互为同分异构体;结构相似、分子组成相差一个或多个CH2基团的有机物互为同系物,①CH3CH2CH2CH3为烷烃,分子式为C4H10,②CH3CH2CH3也是烷烃,分子式为C3H8,二者结构相似、组成相差一个CH2,所以①②互为同系物,④CH3COOH是一元羧酸,分子式为C2H4O2,⑤CH3CH2COOH是一元羧酸,分子式为C3H6O2,二者结构相似、组成相差一个CH2,所以④⑤互为同系物;分子中含有醇羟基的为醇,③CH3CH2OH和⑥![]() 中均含有醇羟基,所以属于醇的是③⑥,核磁共振氢谱吸收峰有4组,说明有4种位置的H原子,且面积比为1:2:2:3,说明这4种位置的H原子个数比为1:2:2:3,符合条件的只有⑦
中均含有醇羟基,所以属于醇的是③⑥,核磁共振氢谱吸收峰有4组,说明有4种位置的H原子,且面积比为1:2:2:3,说明这4种位置的H原子个数比为1:2:2:3,符合条件的只有⑦![]() ,故答案为:⑥⑦、⑧⑨;①②、④⑤;③⑥;⑦。
,故答案为:⑥⑦、⑧⑨;①②、④⑤;③⑥;⑦。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案【题目】在温度相同、容积均为2L的三个恒容密闭容器中,按不同方式投入反应物,发生反应:N2(g)+3H2(g) ![]() 2NH3(g)△H= -92.4kJ/mol;保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是( )
2NH3(g)△H= -92.4kJ/mol;保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是( )
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1molN2、3molH2 | 2molN2、6molH2 | 2molNH3 |
NH3 的浓度(mol/L) | c1 | c2 | c3 |
反应的能量变化 | 放出Q1kJ | 放出Q2kJ | 吸收Q3kJ |
体系压强 | p1 | p2 | p3 |
反应物转化率 |
|
|
|
A. 2p1=2p3<p2 B. 达到平衡时丙容器中NH3的体积分数最大
C. Q3+92.4![]() =92.4 D.
=92.4 D. ![]() <1
<1
【题目】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环,有效降低碳排放。
(1)在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2,一定条件下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJmol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJmol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。
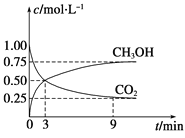
①计算:从0min到3min,H2的平均反应速率v(H2)=_______mol·L-1·min-1,反应至平衡时,放出的热量是_______kJ。
②能说明上述反应达到平衡状态的是________(填编号)。
A.c(CO2) ∶c(CH3OH)=1∶1
B.混合气体的密度不再发生变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
③反应达到平衡后,保持其他条件不变,能加快反应速率且使体系中气体的物质的量减少,可采取的措施有________(填编号)。
A.升高温度 B.缩小容器体积
C.再充入CO2气体 D.使用合适的催化剂
(2)已知A(g)+B(g) ![]() C(g)+D(g) ΔH,反应的平衡常数和温度的关系如下:
C(g)+D(g) ΔH,反应的平衡常数和温度的关系如下:
温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | x | 0.6 | 0.4 |
回答下列问题:
①该反应是_____反应(填“放热”或“吸热”)。
②830℃时,向一个2L的密闭容器中充入0.20mol的A和0.80mol的B,反应至10s时达到平衡,测得A的转化率为80%,计算830℃时,反应的平衡常数x=____。

