题目内容
几种短周期元素的原子半径及主要化合价如下表:

下列叙述正确的是 ( )

下列叙述正确的是 ( )
| A.X、Y元素的金属性 X<Y |
| B.一定条件下,Z单质与W的常见单质直接生成ZW2 |
| C.Y的最高价氧化物对应的水化物能溶于氨水 |
| D.Z的气态氢化物与其最高价氧化物对应的水化物可以反应 |
D
试题分析:A.原子半径越小,原子失去电子就越难,元素的金属性就越弱。所以X、Y元素的金属性 X>Y 。错误。B.由于Z的最高化合价为+5,所以该元素是第ⅤA的元素N,W为第ⅥA的元素O。因为在任何化合物中正负化合价的代数和为0。所以在一定条件下,Z单质与W的常见单质直接生成NO。错误。C.Y是Al,其最高价氧化物对应的水化物Al(OH)3是两性氢氧化物。能跟强酸或强碱发生反应而溶解。但是由于一水合氨是弱碱,所以Al(OH)3不能溶于氨水。错误。D.N的气态氢化物NH3与其最高价氧化物对应的水化物HNO3可以反应生成NH4NO3。正确。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


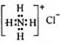
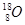
 ,则元素R的原子序数是( )。
,则元素R的原子序数是( )。