题目内容
【题目】我国第五套人民币中的一元硬币材料为钢芯镀镍,依据你所掌握的电镀原理,你认为在硬币制作时,钢芯应做( )
A. 阴极 B. 阳极 C. 正极 D. 负极
【答案】A
【解析】钢芯镀镍时,根据电镀原理,镀件钢芯作阴极,镀层金属镍作阳极,故选A。

 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案【题目】某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
实验一 配制并标定醋酸溶液的浓度
取冰醋酸配制250 mL 0.2 mol/L醋酸溶液,用0.2 mol/L的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
(1)配制250 mL 0.2 mol/L醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和 。
(2)为标定某醋酸溶液的准确浓度,用0.2000 mol/L NaOH溶液对20.00 mL醋酸溶液进行滴定(酚酞作指示剂),几次滴定消耗NaOH溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗NaOH溶液的体积(ml) | 20.05 | 20.00 | 18.80 | 19.95 |
则该醋酸溶液的准确浓度为 mol/L。(保留小数点后四位)
(3)判断滴定终点的方法是 。
(4)下列操作中可能使所测醋酸溶液的浓度数值偏低的是 (填字母序号)。
A.碱式滴定管未用标准液润洗就直接注入标准液
B.滴定前盛放醋酸溶液的锥形瓶用蒸馏水洗净后没有干燥
C.碱式滴定管在滴定前有气泡,滴定后气泡消失
D.量取醋酸体积时,开始俯视读数,滴定结束时仰视读数
实验二 探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸的pH,结果如下:
醋酸浓度(mol·L-1) | 0.0010 | 0.0100 | 0.0200 | 0.1000 |
pH | 3.88 | 3.38 | 3.23 | 2.88 |
(5)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是 。
【题目】酸性KMnO4溶液与H2C2O4溶液的反应通常用来研究浓度对反应速率的影响。现有甲、乙两个实验小组设计不同的实验方案如下:
甲组:改变反应物的浓度,通过溶液褪色的时间来比较反应速率快慢。
可以使用的试剂有:① 0.01mol/L KMnO4酸性溶液、② 0.02mol/L KMnO4酸性溶液、③ 0.1 mol/L H2C2O4溶液、④ 0.2 mol/L H2C2O4溶液。
(1)酸性KMnO4溶液与H2C2O4溶液反应的离子方程式为:__________________________;
(2)请从上面的四种溶液中选择本实验所需的三种溶液(填写序号)_______________;
(3)问题讨论:已知该实验过程中溶液温度几乎不变,但是依据实验数据发现开始一段时间后速率却在增大。
①你认为引起该反应速率增大的因素是_____________________。
②欲设计实验确认,请完成以下设计表a、b、c(褪色时间不需填写):
实验 编号 | 0.01mol/LKMnO4酸性溶液/mL | 0.2mol/L H2C2O4溶液/mL | MnSO4 固体/g | 褪色 时间/s |
1 | 4mL | 2 mL | a | |
2 | b | c | 0.2 g |
乙组:通过测定不同浓度的溶液生成CO2气体体积的方法来比较化学反应速率的大小。
实验装置如图,实验时分液漏斗中A溶液一次性放入B溶液中
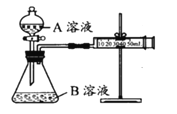
已知乙组完成两次实验分别是Ⅰ、Ⅱ。请完成以下各空:
(4)如何检查该装置的气密性:___________________。
(5)分析所给实验仪器,实现该实验目的还欠缺的仪器:_________________。你将如何比较Ⅰ、Ⅱ化学反应速率大小?你的操作是_________________________。
