题目内容
常温下,用 0.1000 mol/L NaOH溶液滴定 20.00mL 0.1000 mol/L CH3COOH溶液所得滴
定曲线如图。下列说法不正确的是

定曲线如图。下列说法不正确的是

| A.a点所示溶液中:c(Na+)=c(CH3COOH) + c(CH3COO-) |
| B.b和c点所示溶液中:c(OH-)-c(H+)=c(Na+)-c(CH3COO-) |
| C.d点所示溶液中:c(Na+) >c(CH3COO-) >c(OH-) >c(H+) |
| D.滴定过程中可能出现:c(CH3COOH) >c(CH3COO-) >c(H+)> c(Na+)>c(OH-) |
A
试题分析:A、a点时氢氧化钠不足,所示溶液是醋酸钠和醋酸的混合液,所以c(Na+)<c(CH3COOH) + c(CH3COO-),错误;B、b、c对应的溶液中都含有H+、OH-、Na+、CH3COO-,根据电荷守恒,得c(OH-) +c(CH3COO-)=c(Na+)+c(H+),即 c(OH-)-c(H+)=c(Na+)-c(CH3COO-),正确;C、d点时氢氧化钠过量,所示溶液为氢氧化钠与醋酸钠的混合液,溶液呈碱性,所以c(Na+) >c(CH3COO-) >c(OH-) >c(H+) ,正确;D、刚刚滴入很少量的氢氧化钠溶液时,溶液中可能出现c(CH3COOH) >c(CH3COO-)>c(H+)>c(Na+)>c(OH-),正确,答案选A。

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
 H2CO3
H2CO3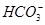 使人体内血液pH保持在7.35~7.45之间,否则就会发生酸中毒或碱中毒。其pH随c(
使人体内血液pH保持在7.35~7.45之间,否则就会发生酸中毒或碱中毒。其pH随c(