题目内容
【题目】如图所示是铝箔在氧气中燃烧的实验,请回答下列问题:
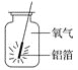
(1)铝在氧气中燃烧的化学方程式为______________________。
(2)实验时要在铝箔上系上一根火柴,其作用是______________________。
(3)集气瓶底部铺上一层细沙,其作用是______________________。
(4)实验中应观察到的现象是______________________________。
(5)用正确方法引燃铝箔,伸入装有氧气的集气瓶中后,未观察到铝箔剧烈燃烧的现象,可能的原因是______。
【答案】4Al+3O2![]() 2Al2O3 点燃火柴从而引燃铝箔 防止高温产物炸裂集气瓶 剧烈燃烧,发出白光,生成白色固体 铝箔表面有一层氧化膜未除去,氧气不纯等
2Al2O3 点燃火柴从而引燃铝箔 防止高温产物炸裂集气瓶 剧烈燃烧,发出白光,生成白色固体 铝箔表面有一层氧化膜未除去,氧气不纯等
【解析】
根据金属铝的物理和化学性质分析解答。
(1)铝在氧气中燃烧生成Al2O3,故方程式为:4Al+3O2![]() 2Al2O3;
2Al2O3;
(2)铝箔上系上一根火柴,作用是点燃火柴从而引燃铝箔;
(3)集气瓶底部铺上一层细沙,作用是防止反应产生的高温产物炸裂集气瓶;
(4)铝在氧气中剧烈燃烧,发出白光,生成白色固体;
(5)铝箔未剧烈燃烧,可能原因是铝箔表面有一层氧化膜未除去,或氧气不纯等。

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目