题目内容
1.航天燃料从液态变为固态,是一项重要的技术突破.铍是高效率的火箭材料,燃烧时放出巨大的能量,已知1kg金属铍完全燃烧放出的热量为62700kJ.则铍燃烧的热化学方程式正确的是( )| A. | Be+$\frac{1}{2}$O2═BeO△H=-564.3kJ•mol-1 | |
| B. | Be(s)+$\frac{1}{2}$O2(g)═BeO(s)△H=+564.3kJ•mol-1 | |
| C. | Be(s)+$\frac{1}{2}$O2(g)═BeO(s)△H=-564.3kJ•mol-1 | |
| D. | Be(s)+$\frac{1}{2}$O2(g)═BeO(g)△H=-564.3kJ•mol-1 |
分析 1kgBe的物质的量为$\frac{1000g}{9g/mol}$=$\frac{1000}{9}$mol,每千克的铍完全燃烧放出的热量为62700kJ,则1mol铍完全燃烧放出的热量为$\frac{62700}{\frac{1000}{9}}$KJ=564.3KJ,根据热化学方程式的书写方法可知,应注意化学计量数与反应热的对应关系及各物质的聚集状态来解答.
解答 解:1kgBe的物质的量为为$\frac{1000g}{9g/mol}$=$\frac{1000}{9}$mol,每千克的铍完全燃烧放出的热量为62700kJ,则1mol铍完全燃烧放出的热量为$\frac{62700}{\frac{1000}{9}}$KJ=564.3KJ,Be与氧气反应生成BeO,其反应方程式为:Be+$\frac{1}{2}$O2═BeO;所以其热化学方程式为:Be(s)+$\frac{1}{2}$O2(g)═BeO(s)△H=-564.3 kJ•mol-1,
故选C.
点评 本题主要考查了反应热的计算,热化学方程式的书写,需要注意的有:物质的状态、反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比.

练习册系列答案
相关题目
12.0.5molCH4完全燃烧生成CO2和液态H2O时,放出445kJ热量,则CH4燃烧热的热化学方程式是( )
| A. | 2CH4(g)+4O2(g)═2CO2(g)+4H2O(1)△H=+890kJ•mol-1 | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=+890 kJ•mol-1 | |
| C. | $\frac{1}{2}$CH4(g)+O2(g)═$\frac{1}{2}$CO2(g)+H2O(g)△H=-445 kJ•mol-1 | |
| D. | CH4(g)+2O2(g)═CO2(g)+2H2O(1)△H=-890 kJ•mol-1 |
9.已知在25℃下,101kPa下,1g辛烷C8H18燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )
| A. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(g)△H=-48.40kJ•mol-1 | |
| B. | 2C8H18(l)+25O2(g)═16CO2(g)+18H2O(g)△H=+11035.2kJ•mol-1 | |
| C. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=+5517.6kJ•mol-1 | |
| D. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=-5517.6kJ•mol-1 |
16.向2.0L恒容密闭容器中充入1.0mol PCl5,在温度为T时发生如下反应PCl5(g)?PCl3(g)+Cl2(g)△H=+124kJ•mol-1.反应过程中测定的部分数据见下表:
回答下列问题:
(1)反应在前50s的平均速率v(PCl5)=0.0016mol/(L•s).
(2)温度为T时,该反应的化学平衡常数=0.025.
(3)上述反应到达平衡状态时,PCl3的体积分数为16.7%.
要提高平衡时PCl3的体积分数,可采取的措施有CD.
A.温度不变,压缩容器体积增大压强 B.使用高效催化剂
C.温度和体积不变,减小PCl5的起始量 D.体积不变,提高反应温度
(4)在温度为T时,若起始时向容器中充入0.5mol PCl5和a mol Cl2平衡时PCl5的转化率仍为20%,则a=0.1.
(5)在热水中,五氯化磷完全水解,生成磷酸(H3PO4),该反应的化学方程式是PCl5+4H2O=H3PO4+5HCl.
| 时间t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
(1)反应在前50s的平均速率v(PCl5)=0.0016mol/(L•s).
(2)温度为T时,该反应的化学平衡常数=0.025.
(3)上述反应到达平衡状态时,PCl3的体积分数为16.7%.
要提高平衡时PCl3的体积分数,可采取的措施有CD.
A.温度不变,压缩容器体积增大压强 B.使用高效催化剂
C.温度和体积不变,减小PCl5的起始量 D.体积不变,提高反应温度
(4)在温度为T时,若起始时向容器中充入0.5mol PCl5和a mol Cl2平衡时PCl5的转化率仍为20%,则a=0.1.
(5)在热水中,五氯化磷完全水解,生成磷酸(H3PO4),该反应的化学方程式是PCl5+4H2O=H3PO4+5HCl.
6.在25℃、101kPa时,充分燃烧一定量的甲醇,放出热量Q kJ(Q>0),经测定完全吸收生成的二氧化碳需要消耗5mol•L-1的KOH溶液100mL,恰好生成正盐.则此条件下,下列热化学方程式正确的是( )
| A. | CH3OH(l)+2O2(g)═CO2(g)+2H2O(l)△H=-2Q kJ•mol-1 | |
| B. | CH3OH(l)+2O2(g)═CO2(g)+2H2O(l)△H=-4Q kJ•mol-1 | |
| C. | CH3OH(l)+2O2(g)═CO2(g)+2H2O(l)△H=-Q kJ•mol-1 | |
| D. | CH3OH(l)+2O2(g)═CO2(g)+2H2O(g)△H=-4Q kJ•mol-1 |
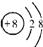 ,写出E的氢化物的分子式:H2O、H2O2.
,写出E的氢化物的分子式:H2O、H2O2.