题目内容
【题目】硫酸铵可用作肥料,也可用于纺织、皮革、医药等方面。某化学兴趣小组对硫酸铵的一些性质进行探究。回答下列问题:
(1)在试管中加入少量硫酸铵样品,加水溶解,滴加NaOH溶液。将湿润的红色石蕊试纸放在试管口,试纸颜色无明显变化。再将试管加热,试纸很快变蓝。由此可知:______________________________________、_________________________________。
(2)从废铁屑中回收铁屑,用碱溶液洗净之后,再用过量硫酸溶解。然后加入稍过量硫酸铵饱和溶液。在小火下蒸发溶剂直到晶膜出现,停火利用余热蒸发溶剂。过滤后用少量乙醇洗涤,得到硫酸亚铁铵晶体。
①碱溶液洗涤的目的是__________________________________。
②硫酸过量的原因是___________________________________。
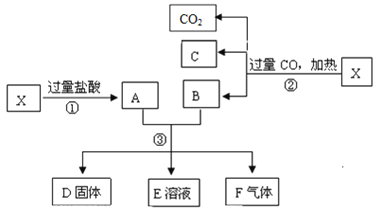
(3)硫酸铵高温下完全分解生成氨气和其他几种气体(含硫产物只有一种)。为探究硫酸铵的其他分解产物,通过下列装置进行实验,通入分解产物一段时间后,再点燃装置E中的酒精灯并开始用装置F收集气体。实验中观察到E中无明显现象,F中排水收集的气体能使燃着的木条熄灭,经测定其相对分子质量为28。
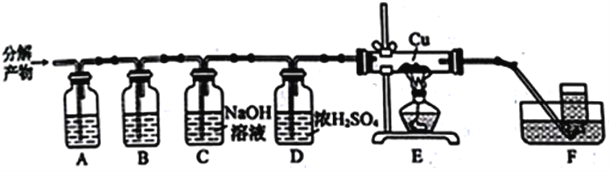
①装置A、B中的溶液分别是______(填标号)。B中可观察到的现象是_____________________。
a.NaOH溶液 b.硫酸溶液 c.BaCl2溶液 d.品红溶液
②装置E的作用是__________________________________。
③写出(NH4)2SO4高温分解的化学方程式:________________________________________。
【答案】NH4+与OH-反应生成的NH3·H2O在加热条件下分解生成NH3, NH3溶于水呈碱性除去铁屑表面的油污抑制Fe2+水解b、d溶液红色变浅(或褪色)验证硫酸铵分解产物中是否存在氧气3(NH4)2SO4![]() 4NH3↑+N2↑+3SO2↑+6H2O↑
4NH3↑+N2↑+3SO2↑+6H2O↑
【解析】
(1)在试管中加入少量硫酸铵样品,加水溶解,滴加NaOH溶液。将湿润的红色石蕊试纸放在试管口,试纸颜色无明显变化,再将试管加热,试纸很快变蓝,说明硫酸铵溶液和NaOH溶液反应生成一水合氨,一水合氨在加热条件下分解生成NH3, NH3溶于水呈碱性;
(2)碱溶液可以洗涤铁屑表面的油污;硫酸亚铁铵溶液因Fe2+、NH4+水解显酸性,过量的硫酸可以抑制Fe2+、NH4+水解;
(3)由题意,F中排水收集的气体能使燃着的木条熄灭,经测定其相对分子质量为28可知F中排水收集的气体是氮气,硫酸铵高温下完全分解生成氮气,说明氮元素化合价升高,则硫酸根中的硫元素化合价一定降低,E中无明显现象说明混合气体中一定没有氧气,说明混合气体中一定存在二氧化硫,则硫酸铵的分解产物为氨气、氮气、二氧化硫和水,反应的化学方程式为:3(NH4)2SO4![]() 4NH3↑+N2↑+3SO2↑+6H2O↑;探究硫酸铵的其他分解产物时,一定要排除氨气对二氧化硫检验的干扰,A中硫酸溶液吸收氨气,排除氨气对二氧化硫检验的干扰,B中品红溶液检验二氧化硫。
4NH3↑+N2↑+3SO2↑+6H2O↑;探究硫酸铵的其他分解产物时,一定要排除氨气对二氧化硫检验的干扰,A中硫酸溶液吸收氨气,排除氨气对二氧化硫检验的干扰,B中品红溶液检验二氧化硫。

【题目】在恒容密闭容器中通入A、B两种气体,在一定条件下发生反应:
2A(g)+B(g)![]() 2C(g) ΔH>0。
2C(g) ΔH>0。
达到平衡后,改变一个条件(x),下列量(y)一定符合图中曲线的是( )
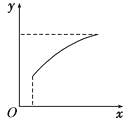
选项 | x | y |
A | 再通入A | B的转化率 |
B | 加入催化剂 | A的体积分数 |
C | 压强 | 混合气体的总物质的量 |
D | 温度 | 混合气体的总物质的量 |
【题目】铬铁矿主要成分为FeO、Cr2O3,含有SiO2、Al2O3等杂质。工业上用铬铁矿制备红矾钠晶体(Na2Cr2O7)的流程如图所示:
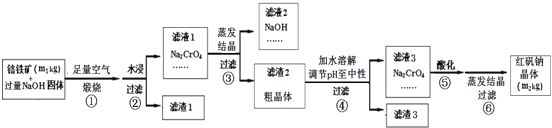
(1)步骤①的主要反应为FeO·Cr2O3+O2+NaOH![]() Na2CrO4+NaFeO2+H2O,该反应配平后FeO·Cr2O3与O2的系数比为___________。该步骤是在坩埚中进行煅烧,可用此坩埚材料的是______________(填标号)。
Na2CrO4+NaFeO2+H2O,该反应配平后FeO·Cr2O3与O2的系数比为___________。该步骤是在坩埚中进行煅烧,可用此坩埚材料的是______________(填标号)。
A.铁 B.氧化铝 C.石英 D.陶瓷
(2)步聚①煅烧反应极慢,需要升温至NaOH呈熔融状态,反应速率才加快,其原因是____________________________________________________。
(3)步骤②中NaFeO2会强烈水解生成氢氧化铁沉淀,反应的化学方程式为________________。
(4)将五份滤液1分别在130℃蒸发1小时,各自冷却到不同温度下结晶,保温过滤,所得实验数据如下表。根据数据分析,步骤③的最佳结晶温度为___________℃。
结晶温度/℃ | Na2CrO4粗晶中各物质含量/% | |||
Na2CrO4 4H2O | NaOH | NaAlO2 | Na2SiO3 | |
30 | 52.45 | 29.79 | 8.69 | 12.21 |
40 | 68.81 | 20. 49 | 8.46 | 10.84 |
50 | 60.26 | 27. 96 | 10.36 | 9.32 |
60 | 50.74 | 29.66 | 10.40 | 12.25 |
70 | 46.77 | 33.06 | 8.10 | 6.48 |
(5)步骤④中滤渣3的成分是_____________(写化学式)。
(6)若该流程中铬元素完全转化为红矾钠晶体,则该铬铁矿中铬元素的质量分数为____________(用含m1、m2的代数式表示)。