��Ŀ����
��10�֣���ҵ����MnO2��KOHΪԭ����ȡ������أ���Ҫ�������̷��������С���һ����MnO2����KOH���飬��Ͼ��ȣ��ڿ����м������ۻ������������裬��ȡK2MnO4���ڶ�����K2MnO4��Ũ��Һ���е�⣬��ȡKMnO4���Իش��������⣺
��1����ȡK2MnO4��MnO2����һ������ԭ��Ӧ��_____________�������������ԭ���������������Ŀ����________________________________��
��2�����K2MnO4��Ũ��Һʱ�����������ĵ缫��ӦʽΪ��
������_______________________,
������_________________________��
����ܵķ�Ӧ����ʽ��_________________________��
��10�֣�ÿ��2�֣���1����ԭ�����������ֽӴ���ʹMnO2������ȫ
��2��2H++2e-==H2����MnO42��-e-=== MnO4-,2K2MnO4+2H2O==2KMnO4+2KOH+H2��
����:��

 �����Ļ�������ҵϵ�д�
�����Ļ�������ҵϵ�д���19�֣�����������̵���Ҫ������ͳ��õ���������������ʵ������ģ�ҵ�������̿��Ʊ�������ص�����ͼ��
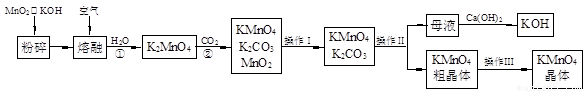
��1�������������Ϊ �������������Ϊ ��
��2����Ӧ�ڵĻ�ѧ����ʽΪ ����ҵ��������ԭ������KMnO4�������ʽϵͣ��Ϻõ��Ʊ������ǵ�ⷨ����Pt��������Fe��������K2MnO4Ϊ���Һ�������ĵ缫��ӦʽΪ ��
��3��KMnO4��һ�ֽ��ȶ��Ļ�������չ��KMnO4��Һ�ķֽ��д����ã�����MnO2��KOH��O2���� MnO2Ҳ�Ǹ÷ֽⷴӦ��һ�ִ������������һ��ʵ�鷽������֤MnO2�Ը÷ֽⷴӦ���д��ԣ� ��
��4��KMnO4�����Խ����е�ǿ�����Թ㷺Ӧ���ڷ�����ѧ�С�
���磺2KMnO4+3H2SO4+5Na2SO35Na2SO4+K2SO4+2MnSO4+3H2O��ijͬѧ��KMnO4�ⶨʵ���ҳ��ڴ�ŵ�Na2SO3����Ĵ��ȡ�����ȷ��ȡ6.3 g Na2SO3������Ʒ�����500 mL��Һ��ȡ25.00 mL������Һ������ƿ�У���0.01000 mol/L ������KMnO4��Һ���еζ����ζ�������±���ʾ��
|
�ζ�����[��Դ:][��Դ:Z&xx&k.Com] |
������Һ�����/mL[��Դ:ѧ#��#��Z#X#X#K] |
����Һ�����[��Դ:] |
|
|
�ζ�ǰ�̶�/mL |
�ζ���̶�/mL |
||
|
1 |
25.00 mL |
0.02 |
24.01 |
|
2 |
25.00 mL |
0.70 |
24.71 |
|
3 |
25.00 mL |
0.20 |
24.20 |
������500 mLNa2SO3��Һʱ�������õ���ʵ�������У��ձ�������������ͷ�ιܡ�ҩ�� �� ��
���жϵζ��յ�������� ��
�����в����ᵼ�²ⶨ���ƫ�ߵ���
A��δ�ñ�Ũ�ȵ�����KMnO4��Һ��ϴ�ζ���
B���ζ�ǰ��ƿδ����
C���ζ�ǰ�ζ��ܼ��첿��������
D���۲����ʱ���ζ�ǰ���ӣ��ζ�����
��������ʵ�����ݣ�����Na2SO3�Ĵ���Ϊ ��
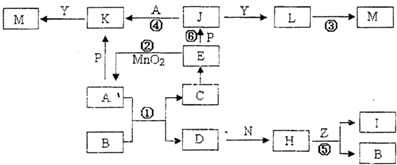
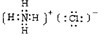
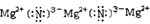
 MnCl2+Cl2+2H2O�� KClO3+6HCl��Ũ����KCl+3Cl2+3H2O��������ȫ�ܽ���ռ���15.68L��Cl2����״���£�����Cl2����ģ�����������и������ʵ�������______��
MnCl2+Cl2+2H2O�� KClO3+6HCl��Ũ����KCl+3Cl2+3H2O��������ȫ�ܽ���ռ���15.68L��Cl2����״���£�����Cl2����ģ�����������и������ʵ�������______��