题目内容
4.下列各组离子,在强碱性溶液中可以大量共存的是( )| A. | K+ HCO3- NO3- ClO- | B. | Na+ SO32- NH4+ Ba2+ | ||
| C. | Ba2+ S2- Cl- SO42- | D. | AlO2- CO32- Cl- Na+ |
分析 强碱性溶液中存在大量氢氧根离子,
A.碳酸氢根离子与氢氧根离子反应生成碳酸根离子和水;
B.亚硫酸根离子与钡离子反应生成亚硫酸钡沉淀,铵根离子与氢氧根离子反应生成弱电解质一水合氨;
C.钡离子与硫酸根离子反应生成难溶物硫酸钡;
D.四种离子之间不反应,都不与强碱性溶液反应.
解答 解:A.HCO3-与强碱性溶液中的氢氧根离子反应,在溶液中不能把大量共存,故A错误;
B.SO32-、Ba2+之间反应生成亚硫酸钡,NH4+与强碱性溶液反应,在溶液中不能大量共存,故B错误;
C.Ba2+、SO42-之间反应生成硫酸钡沉淀,在溶液中不能大量共存,故C错误;
D.AlO2- CO32- Cl- Na+之间不发生反应,都不与强碱性溶液中的氢氧根离子反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,题目难度中等,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;试题侧重对学生基础知识的训练和检验,有利于培养学生灵活运用基础知识的能力

练习册系列答案
相关题目
14.分别向下列各溶液中加入少量NaOH固体,溶液的导电能力变化最小的是( )
| A. | 水 | B. | 盐酸 | C. | 醋酸溶液 | D. | NaCl溶液 |
12.若M+N=F+G这一反应是放热反应,下列说法正确的是( )
| A. | M的能量比G高 | |
| B. | N的能量比G高 | |
| C. | 这一反应不需要加热一定能发生 | |
| D. | 反应物的能量之和大于生成物的能量之和 |
19.2006年,发生在山西等地的瓦斯爆炸事故,造成多人伤亡,因此在矿井里,必须采取安全措施,如通风、严禁烟火等,而且要随时检查瓦斯的体积分数,当空气中混有5%---15%的甲烷时,遇到明火会发生爆炸,当爆炸最强烈时,甲烷的含量(体积分数)为( )(设空气中氧气含量为20%)
| A. | 9.1% | B. | 10.5% | C. | 10% | D. | 5% |
16.下列离子方程式错误的是( )
| A. | 硫酸氢钠溶液中加入氢氧化钠溶液:H++OH-=H2O | |
| B. | 氧化铜和稀盐酸:CuO+2H+=Cu2++H2O | |
| C. | 少量的NaHCO3与足量的NaOH溶液:HCO3-+OH-=CO32-+H2O | |
| D. | 少量的NaHCO3溶液与足量的Ca(OH)2溶液:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
13.以石墨为电极,电解1L CuSO4和NaCl的混合溶液,其中CuSO4与NaCl的物质的量之和为0.2mol,CuSO4的物质的量占总物质的量的比值为a.下列说法正确的是( )
| A. | 若a=0.5,当Cu2+在阴极恰好全部析出时,产生的气体只有氯气 | |
| B. | 若a=0.5,当Cu2+在阴极恰好全部析出时,产生的气体的物质的量为0.1mol | |
| C. | 若a=0.2,当Cl-在阳极恰好全部逸出时,产生0.08mol的NaOH | |
| D. | 若电解一段时间后,阴、阳两极产生的气体的物质的量恰好均为0.16mol,则a=0.2 |
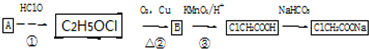
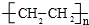 .
.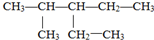 的名称是2-甲基-3-乙基戊烷;
的名称是2-甲基-3-乙基戊烷;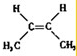 ;
;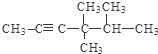 .
.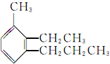 的系统名称为3-甲基-2-乙基丙苯.
的系统名称为3-甲基-2-乙基丙苯.