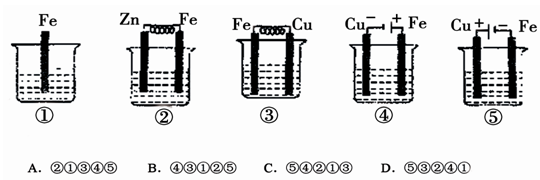
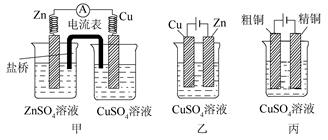
题目内容
如图用石墨作电极的电解池中,放入某足量蓝色溶液500mL进行电解,观察到A电极表面有红色固体生成,B电极有无色气体生成;通电一段时间后,取出A电极,洗涤、干燥、称量,A电极增重1.6g。下列说法错误的是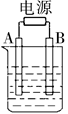
| A.图中B极同电源正极相连 |
| B.该蓝色溶液可能是Cu(NO3)2或CuCl2溶液[ |
| C.电解后溶液的pH约为 1(溶液体积变化忽略不计) |
| D.要使电解后溶液恢复到电解前的状态,则可加入2 g CuO |
B
解析试题分析:根据现象判断蓝色溶液可为硫酸铜或硝酸铜溶液,A、电解时铜在阴极析出,氧气在阳极产生,B与电源的正极相连,正确;B、若电解CuCl2溶液阳极产生黄绿色气体,错误;C、根据电荷守恒,析出铜单质,氢离子补充,n(H+)="2" n(Cu2+)=2×1.6÷64=0.05mol,c(H+)=0.1mol/L,正确;D、电解时产生铜和氧气,加入n(CuO)= 1.6÷64×80=2g,正确。
考点:考查电解池原理有关问题。

练习册系列答案
相关题目
如图是一种可充电的锂离子电池充、放电的工作示意图。该电池的反应式为:LiMnO2 + C6 Li1-x MnO2 + LixC6 (LixC6表示锂原子嵌入石墨形成的复合材料)下列有关说法正确的是
Li1-x MnO2 + LixC6 (LixC6表示锂原子嵌入石墨形成的复合材料)下列有关说法正确的是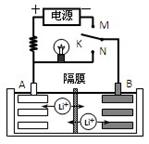
| A.K与N相接时,A极为负极,该电极反应式为:LixC6 - xeˉ= C6 + xLi+ |
| B.在整个充电或放电过程中都只存在一种形式的能量转化 |
| C.K与N相接时,Li+由A极区迁移到B极区 |
| D.K与M相接时,A极发生氧化反应,LiMnO2 -xeˉ = Li1-xMnO2 + xLi+ |
镁—H2O2酸性燃料电池采用海水作电解质(加入一定量的酸),下列说法正确的是
| A.电池总反应为Mg+H2O2 = Mg(OH)2 |
| B.正极发生的电极反应为H2O2+2H++2e- = 2H2O |
| C.工作时,正极周围海水的pH减小 |
| D.电池工作时,溶液中的H+向负极移动 |
有关下图的说法正确的是( )
| A.a和b连接构成原电池,溶液中SO42-移向Cu极 |
| B.a和b连接构成原电池,Cu极上发生还原反应 |
| C.a、b分别接直流电源正、负极,电子从Cu片流向b |
| D.a、b分别接直流电源正、负极,可以在Fe片上镀Cu |
下列各变化中属于原电池反应的是
| A.在空气中金属铝表面迅速氧化形成保护层 |
| B.镀锌铁表面有划损时,也能阻止铁被氧化 |
| C.红热的铁丝与冷水接触,表面形成蓝黑色保护层 |
| D.浓硝酸比稀硝酸更能氧化金属铜 |
有关右图电化学装置的叙述中,正确的是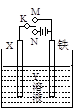
| A.若X为碳棒,Y为饱和食盐水,K置于N,则铁极上析出氯气 |
| B.若X为铂棒,Y为CuCl2溶液,K置于N,则铁棒质量将增加 |
| C.若X为锌棒,Y为海水,K置于M,形成对铁的外加电流阴极保护 |
| D.若X为铜棒,Y为稀硫酸,K置于M,则正极反应为:Fe?2e→Fe2+ |
串联电路中四个电解池分别装有0.5 mol·L-1的下列溶液,用惰性电极电解,连接直流电源一段时间后,溶液pH最小的是( )
| A.KNO3溶液 | B.NaCl溶液 | C.AgNO3溶液 | D.CuCl2溶液 |