题目内容
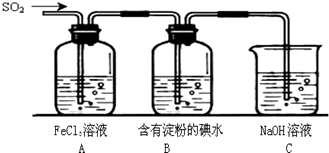
为了降低硫氧化物造成的空气污染,一种方法是在含硫燃料(如煤)燃烧过程中加入生石灰,这种方法叫“钙基固硫”,采用这种方法在燃料燃烧过程中的“固硫”反应方程式为:
SO2+CaO══CaSO3 ; 2 CaSO3+O2=2 CaSO4
试题分析:煤在燃烧的过程中加入生石灰,可以达到脱硫的目的,煤中的S燃烧生成二氧化硫,儿童含量与CaO反应生成亚硫酸钙,亚硫酸钙与空气中的氧气反应最终生成硫酸钙,化学方程式为SO2+CaO══CaSO3 ; 2 CaSO3+O2=2 CaSO4

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案
相关题目

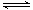 NO + SO3,在体积为VL的密闭容器中通入amolNO2和bmolSO2,反应后容器内硫原子和氧原子的个数比为( )
NO + SO3,在体积为VL的密闭容器中通入amolNO2和bmolSO2,反应后容器内硫原子和氧原子的个数比为( )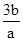
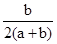
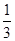
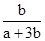
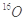 和
和