题目内容
已知A、B、C、D为短周期主族元素,其相对位置关系如图。C与B可形成离子化合 物C3B2。下列分析正确的是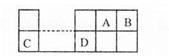
A.电负性:C>A
B.离子氧化性:C>D
C.氢化物稳定性:A> B
D.原子半径:r(C)> r(B)
D
解析试题分析:离子化合物C3B2中C和B的化合价分别为+2和-3,所以C和B分别为Mg和N。则A为C、D为Al。A、同周期元素从左向右,电负性增大;同主族元素从上到下,电负性减小。电负性Be<C,Be>Mg,错误;B、还原性Mg>Al,氧化性:Mg2+<Al3+,错误;C、非金属性:N>C,稳定性:NH3>CH4,错误;D、原子半径:Mg>(Be)>N,正确。
考点: 元素周期律 元素周期表

 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案甲、乙、丙、丁四种短周期主族元素,它们的价电子数依次增大,乙形成的化合物种类最多,甲与乙的原子序数之和等于丁的原子序数,丙和乙位于同一周期,丁和乙位于不同周期。则下列说法中正确的是
| A.甲、乙、丙形成的化合物既有离子键又有共价键 |
| B.乙、丙、丁形成的氢化物常温下均为气体 |
| C.原子序数由小到大顺序为:甲<乙<丙<丁 |
| D.原子半径大小顺序为:丁>甲>乙>丙 |
短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是电子层数的三倍,Y与X可形成Y2X2和Y2X两种离子化合物,Z原子的核外电子数比Y原子多1,W与X同主族,则
| A.原子半径:Y< Z < W |
| B.单质的还原性:Y> Z |
| C.气态氢化物的稳定性:X>W |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
短周期元素X、Y、Z、R在周期表中的位置如图。下列说法正确的是
| | | ||||
| | | X | Y | | |
| | | | Z | R | |
A.气态氢化物的稳定性:X > Y
B.原子半径大小:Y> Z
C.X和Y形成的化合物是离子化合物
D.Z、R的最高价氧化物对应的水化物都是强酸
已知某短周期元素原子的第三电子层上排布有5个电子,则该元素在周期表中的位置是( )
| A.第二周期第IVA族 | B.第二周期第VA族 |
| C.第三周期第IVA族 | D.第三周期第VA族 |
X、Y、Z、W四种短周期主族元素原子半径依次减小,其中X、Y、Z位于同一周期,只有X为金属元素,X和Y最外层电子数差1,Y和Z的核电荷数差3,Z与W最外层电子数相同。下列说法正确的是
| A.Y与W形成的化合物一定含有离子键 |
| B.W的氢化物沸点一定大于Z的氢化物沸点 |
C.若形成化合物YZ4,则YZ4的电子式为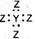 |
| D.若形成化合物XZ3,则XZ3中所有原子均满足最外层8电子稳定结构 |
下列说法中,正确的是
| A.离子化合物中,阴、阳离子间存在静电吸引力 |
| B.HF、HCl、HBr和HI的热稳定性和还原性从左到右依次减弱 |
| C.第三周期非金属元素对应的含氧酸从左到右依次增强 |
| D.短周期元素形成离子后,最外层电子数都达到8电子稳定结构 |
已知a、b分别为同周期的ⅡA族和ⅦA族的两种元素,它们的原子序数分别为m和n,则下列关系不可能成立的是( )
| A.m=" n" —15 | B.n=m+12 | C.m=n —29 | D.n=m+5 |