题目内容
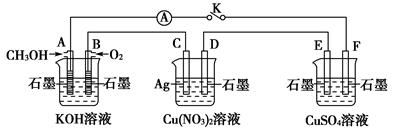
一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧化碳。该电池负极发生的反应是( )
| A.CH3OH(g)+O2(g)-2e-=H2O(l)+CO2(g)+2H+(aq) |
| B.O2(g)+4H+(aq)+4e-=2H2O(l) |
| C.CH3OH(g)+H2O(l)-6e-=CO2(g)+6H+(aq) |
| D.O2(g)+2H2O(l)+4e-=4OH- |
C
首先写出该燃料电池的总反应式:2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(l),然后分析化合价变化,确定氧化反应、还原反应及负正极。因为负极发生氧化反应,故反应式为:2CH3OH(g)+2H2O(l)-12e-=2CO2(g)+12H+(aq);正极发生还原反应,反应式为:3O2(g)+12H+(aq)+12e-=6H2O (l)。

练习册系列答案
相关题目
 NiOOH+MH,下列叙述正确的是 ( )
NiOOH+MH,下列叙述正确的是 ( )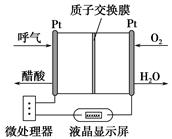
 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH