题目内容
(2012?合肥一模)NaNO2是一种食品添加剂,它能致癌.酸性KMnO4溶液与NaNO2的反应方程式是:MnO
+NO
+K→Mn2++NO
+H2O.下列叙述中正确的是( )
- 4 |
- 2 |
- 3 |
分析:该反应中锰元素化合价由+7价变为+2价,N元素化合价由+3价变为+5价,结合元素守恒、硝酸钠和高锰酸钾之间的关系式分析解答.
解答:解:A.该反应中N元素化合价由+3价变为+5价,所以亚硝酸根离子失电子被氧化,故A错误;
B.根据元素守恒、电荷守恒知,K是H+,氢离子参加反应导致溶液中氢离子浓度降低,则溶液的pH增大,故B错误;
C.根据转移电子守恒得,生成1molNaNO3需消耗KMnO4的物质的量=
=0.4mol,故C正确;
D.根据元素守恒、电荷守恒知,K是H+,故D错误;
故选:C.
B.根据元素守恒、电荷守恒知,K是H+,氢离子参加反应导致溶液中氢离子浓度降低,则溶液的pH增大,故B错误;
C.根据转移电子守恒得,生成1molNaNO3需消耗KMnO4的物质的量=
| 1mol×(5-3) |
| 7-2 |
D.根据元素守恒、电荷守恒知,K是H+,故D错误;
故选:C.
点评:本题考查了氧化还原反应,根据转移电子守恒、电荷守恒、原子守恒配平方程式,结合物质间的反应分析解答,难度中等.

练习册系列答案
相关题目
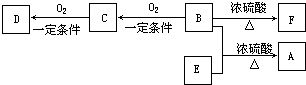 (2012?合肥一模)有机物A(C10H20O2)具有兰花香味.已知:
(2012?合肥一模)有机物A(C10H20O2)具有兰花香味.已知: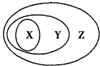 (2012?合肥一模)如图所示的一些物质或概念间的从属关系不正确的是( )
(2012?合肥一模)如图所示的一些物质或概念间的从属关系不正确的是( )