题目内容
许多国家十分重视海水资源的综合利用.不需要化学变化就能够从海水中获得的物质是
| A.氯、溴、碘 | B.钠、镁、铝 | C.烧碱、氢气 | D.食盐、淡水 |
D
解析试题分析:A、氯、溴、碘均是非金属单质,而海水中它们均以离子的形成存在,因此必须通过化学变化才能获得,A不正确;B、钠、镁、铝均活泼的金属单质,它们在海水中它们均以离子的形成存在,因此必须通过化学变化才能获得,B不正确;C、电解氯化钠溶液才能获得氢氧化钠、氢气和氯气,直接从海水不可能获得烧碱、氢气,C不正确;D、海水中含有氯化钠,蒸发即得到食盐。通过海水的淡化可以获得淡水,均是物理变化,D正确,答案选D。
考点:考查海水应用的有关判断

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
广东正在建设海洋强省。下列说法不正确的是
| A.从海带中提取碘单质的过程涉及氧化还原反应 |
| B.往淡水中加入氯化钠等配成人造海水,可用于海产品的长途运输 |
| C.赤潮主要是工农业生产和生活废水引起沿海水域的富营养化而造成的 |
| D.以海水为原料制取镁的过程未发生氧化还原反应 |
下列反应原理不符合工业冶炼金属实际情况的是
A.2HgO 2Hg+O2↑ 2Hg+O2↑ |
B.4Al+3MnO2 2Al2O3+3Mn 2Al2O3+3Mn |
C.2AlCl3 2Al+3Cl2 ↑ 2Al+3Cl2 ↑ |
D.4CO+Fe3O4 3Fe+4CO2 3Fe+4CO2 |
下列金属冶炼的反应原理,错误的是( )
A.2NaCl(熔融) 2Na+Cl2↑ 2Na+Cl2↑ | B.MgO+H2 Mg+H2O Mg+H2O |
C.Fe2O3+3CO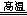 2Fe+3CO2 2Fe+3CO2 | D.2HgO 2Hg+O2↑ 2Hg+O2↑ |
我国有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某些转化步骤及生成物未列出):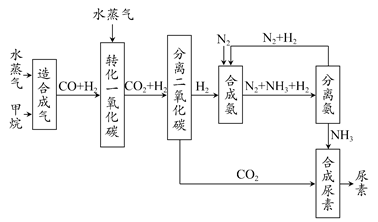
请填写下列空白:
(1)已知0.5 mol甲烷和0.5 mol水蒸气在t ℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量。该反应的热化学方程式是___________。
(2)上述流程中,工业上分离H2、CO2合理的方法是_____________________。
| A.混合气先通入氢氧化钠溶液,再在溶液中加盐酸 |
| B.混合气加压冷却,使CO2液化 |
| C.混合气用氨水洗涤 |
| D.混合气先通入到石灰浆,然后高温煅烧固体 |
在合成氨的实际生产过程中,常采取将生成的氨从混合气体中分离出来,分离出氨的方法:________________。
(4)合理地利用资源不仅可以提高经济效益,而且也是对社会、对全人类负责的表现,请用线段和箭头画出图中的两处合理利用资源情况。
下列金属的冶炼不适宜用热还原法来冶炼的是( )。
| A.铁 | B.铜 | C.钠 | D.铅 |
下列化工生产原理错误的是( )。
①可以电解熔融的氯化钠来制取金属钠 ②可以将钠加入氯化镁饱和溶液中制取镁 ③用电解法冶炼铝时,原料是氯化铝 ④炼铁时高炉中所发生的反应都是放热的,故无需加热
| A.②③ | B.①③ | C.①②③ | D.②③④ |
下列金属一般用电解熔融盐的方法冶炼的是( )。
| A.活动性强的金属 | B.活动性弱的金属 |
| C.人类较早使用的金属 | D.明代作货币的金属 |
下列关于工业生产的说法中,不正确的是( )
| A.工业上,用焦炭在电炉中还原二氧化硅得到含杂质的粗硅 |
| B.生产普通水泥的主要原料有石灰石、石英和纯碱 |
| C.工业上将粗铜电解精炼,应将粗铜连接电源的正极 |
| D.在高炉炼铁的反应中,一氧化碳作还原剂 |