题目内容
【题目】设NA表示阿伏加德罗常数的值。下列叙述正确的是
A.4.0 g由CO2和SO2组成的混合物中含有的质子数为2NA
B.2.24 L Cl2与CH4在光照下反应生成的HCl分子数为0.1NA
C.0.1 mol/L K2S溶液中含有的K+数为0.2NA
D.4.2 g CaH2与水完全反应,转移的电子数为0.1NA
【答案】A
【解析】
A. 4.0 g CO2中含有的质子数为![]() =2NA,4.0 g SO2中含有的质子数为
=2NA,4.0 g SO2中含有的质子数为![]() =2NA,因此4.0 g由CO2和SO2组成的混合物中含有的质子数也为2NA,故A正确;
=2NA,因此4.0 g由CO2和SO2组成的混合物中含有的质子数也为2NA,故A正确;
B. 未指明是否为标准状况,无法计算,故B错误;
C. 没有溶液体积,不能计算0.1 mol/L K2S溶液中的K+数目,故C错误;
D. 4.2 g CaH2与水完全反应,化学方程式为CaH2+2H2O = Ca(OH)2+2H2↑,转移的电子的物质的量为0.2 mol,数目为0.2NA,故D错误。
综上所述,答案为A。

练习册系列答案
相关题目
【题目】向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g) ![]() 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示
容器 | 甲 | 乙 | 丙 |
容积 | 0.5L | 0.5L | 1.0L |
温度/℃ | T1 | T2 | T2 |
反应物起始量 | 0.5molA 1.5 molB | 0.5 molA 1.5 molB | 2.0 molA 6.0 molB |
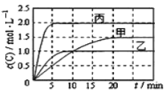
下列说法正确的是
A.由图可知:T1<T2,且该反应为吸热反应
B.T2时该反应的平衡常数K=0.8
C.l0min内甲容器中反应的平均速率v(B)=0.025mol·(L·min)-1
D.T1℃,若起始时甲容器中充入1.5molA、0.5molB,平衡时B的转化率为25%