题目内容
【题目】A、B、C、D、E、X 是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。
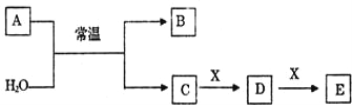
(1)若 A 为常见的金属单质,焰色反应呈黄色,X 能使品红溶液褪色,写出 C 和 E 反应的离子方程式:______________________________。
(2)若 A 为淡黄色粉末,X 为一种最常见的造成温室效应的气体。则鉴别等浓度的 D、E 两种溶液,可 选择的试剂为_____(填代号)。
A.盐酸 B.BaCl2 溶液 C.Ca(OH)2 溶液
(3)若 A 为非金属氧化物,X 是 Fe,溶液 D 中加入 KSCN 溶液变红。则 A 与 H2O 反应的化学反应方程 式为_____。
【答案】OH-+HSO3-=SO32-+H2O AB 3NO2+H2O=2HNO3+NO
【解析】
(1)若A为常见的金属单质,焰色反应呈黄色,应为Na,X能使品红溶液褪色,应为SO2,则B为H2,C为NaOH,D为Na2SO3,E为NaHSO3;
(2)若A为淡黄色粉末,应为Na2O2;若X为一种造成温室效应的气体,应为CO2,以此分析。
(3)若A为非金属氧化物,X是Fe,由转化关系可知C具有强氧化性,则A为NO2,B为NO,C为HNO3。
(1)Na位于周期表第三周期ⅠA族,C和E反应的离子方程式为OH-+HSO3-=SO32-+H2O;
(2)若A为淡黄色粉末,应为Na2O2,若X为一种造成温室效应的气体,应为CO2,则C为NaOH,D为Na2CO3,E为NaHCO3,鉴别等浓度的D、E两种溶液,可用盐酸或氯化钡溶液,用盐酸产生气泡快的为NaHCO3,用氯化钡产生沉淀的为碳酸钠,故选AB。
(3)若A为非金属氧化物,X是Fe,由转化关系可知C具有强氧化性,则A为NO2,B为NO,C为HNO3,D为 Fe(NO3)3,E为 Fe(NO3)2,①NO2与水反应的方程式为3NO2+H2O=2HNO3+NO。

【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表,建立平衡需要的时间为20 s,则下列说法不正确的是
物质 | X | Y | Z |
初始浓度/(mol·L-1) | 0.2 | 0.1 | 0.1 |
平衡浓度/(mol·L-1) | 0.05 | 0.05 | 0.2 |
A. 反应可表示为3X+Y![]() 2Z
2Z
B. 建立平衡过程中,用Z表示的反应速率为v(Z)=0.005 mol·L-1·s-1
C. 增大压强使平衡向生成Z的方向移动,平衡常数增大
D. 若初始浓度:X为0.2 mol·L-1,Y为0.2 mol·L-1,Z为0.8mol·L-1,则平衡向右移动