题目内容
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只能被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )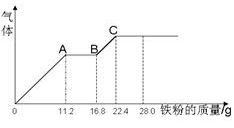
| A.原混合液中NO3-的物质的量为0.4mol |
| B.c(H2SO4)为5mol·L-1 |
| C.溶液中最终溶质为FeSO4 |
| D.OA段产生是NO,AB段反应为2Fe3++Fe = 3Fe2+,BC段产生氢气 |
B
解析试题分析:铜与硝酸溶液反应的离子方程式是:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,n(Cu)=19.2g÷64g/mol=0.3mol,所以n(NO3-)=0.2mol.故原溶液中含硝酸根离子的物质的量是0.4mol.正确。对于另一份溶液来说,发生的反应是:O—A段:Fe+4H++NO3-=Fe3++NO↑+2H2O;A—B段:2Fe3++Fe=3Fe2+;B—C段:Fe+2H+= Fe2++H2↑.反应到最后溶液为FeSO4溶液。在O—A段n(Fe)=0.2mol,消耗的氢离子n(H+)=0.8mol,在B—C段n(Fe)=0.1mol,消耗的氢离子n(H+)=0.2mol,即n(H+)总=0.8mol+0.2mol=1mol.由于n(HNO3)=n(NO3-)=0.2mol,所以n(H2SO4)=(1.0-0.2)mol/2=0.4mol.故C(H2SO4)=0.4mol÷0.1L=4mol/L.所以错误选项为:B。
考点:考查金属Fe、 Cu与硝酸、硫酸的混合溶液的反应及计算的知识。

右图是一种试验某气体化学性质的实验装置。在A处通入氯气,图中B为开关,关闭B时,C中红色布条颜色无变化;打开B时,C处红色布条颜色褪去。由此做出的判断正确的是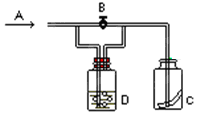
| A.D中可以是水 | B.D中可以是饱和食盐水 |
| C.D中不可能是浓H2SO4 | D.通入的氯气中含有水蒸气 |
①在含有FeCl3和BaCl2的酸性混合液中,通入足量SO2气体,有白色沉淀生成,过滤后,向滤液中滴加KSCN溶液,不出现红色,②在氨水和BaCl2的混合液中,通入适量SO2气体,也有白色沉淀生成,由此得出的结论是
| A.白色沉淀都是BaSO3 |
| B.①白色沉淀是BaSO3和S,②是BaSO3 |
| C.①白色沉淀是BaSO4,②是BaSO3 |
| D.①白色沉淀是FeSO3,②是BaSO3 |
如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是( )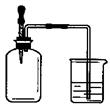
①CO、O2②Cl2、CH4③NO2、O2④N2、H2
| A.①② | B.②④ | C.③④ | D.②③ |
下列有关化学反应过程或实验现象的叙述中,正确的是
| A.氯气的水溶液可以导电,说明氯气是电解质 |
| B.漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 |
| C.氯气可以使湿润的有色布条褪色,但实际起漂白作用的物质是次氯酸而不是氯气 |
| D.为证明氯水中含Cl-,可先加盐酸酸化,再加入AgNO3溶液 |
下列说法不正确的是( )
| A.浓硝酸与足量铜片反应时,先生成红棕色气体,后生成无色气体 |
| B.浓硫酸具有强氧化性,常温下可将铁、铝的单质氧化 |
| C.饱和氯水既有酸性又有漂白性,加入NaHCO?后漂白性减弱 |
| D.浓盐酸与足量二氧化锰反应后,盐酸有剩余 |
如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是
①CO、O2 ②Cl2、CH4 ③NO2、O2 ④N2、H2
| A.①② | B.②④ | C.③④ | D.②③ |
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素
| A.在自然界中只以化合态的形式存在 | B.单质常用作半导体材料和光导纤维 |
| C.最高价氧化物不与任何酸反应 | D.气态氢化物比甲烷稳定 |
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
| A.向NaHCO3固体中加入新制的氯水,有无色气泡产生(H+) |
| B.新制氯水使红色布条褪色(HCl) |
| C.将AgNO3溶液滴加到新制氯水中,有白色沉淀产生(Cl-) |
| D.向FeCl2溶液中滴加新制氯水,再滴加KSCN溶液,溶液呈红色(Cl2) |