题目内容
【题目】H3BO3可以通过电解NaB(OH)4溶液的方法制备,其工作原理如图,下列叙述错误的是
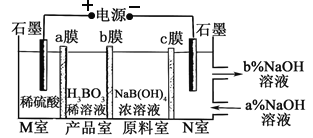
A. M室发生的电极反应式为:2H2O-4e- = O2↑+4H+
B. N室中:a% <b%
C. b膜为阴离子交换膜
D. 理论上每生成1mol产品,阴极室可生成5.6L气体
【答案】D
【解析】A.M室为阳极室,发生氧化反应,其电极反应式为2H2O-4e- = O2↑+4H+,故A正确;B.N室为阴极室,发生的电极反应式为2H2O+2e-=H2↑+2OH-,原料室的Na+透过阳离子交换膜进入阴极室,则NaOH的质量百分数为a% <b%,故B正确;C.电解池工作时,原料室的B(OH)4-透过阴离子交换膜,进入产品室和H+结合生成H3BO3,故C正确;D.理论上每生成1mol产品,转移电子数为1mol电子,阴极室可生成氢气11.2L(标准状况),故D错误;答案为D。

练习册系列答案
相关题目