题目内容
【题目】硫单质和化合物在工农业生产中有着重要的应用,而SO2直接排放会对环境造成危害。
Ⅰ.已知:重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下:
BaSO4(s)+4C(s) ![]() BaS(s)+4CO(g) ΔH=+571.2 kJ·mol1
BaS(s)+4CO(g) ΔH=+571.2 kJ·mol1
BaS(s) ![]() Ba(s)+S(s) ΔH=+460 kJ·mol1
Ba(s)+S(s) ΔH=+460 kJ·mol1
已知:2C(s)+O2(g) ![]() 2CO(g) ΔH=221 kJ·mol1
2CO(g) ΔH=221 kJ·mol1
则:Ba(s)+S(s)+2O2(g) ![]() BaSO4(s) ΔH=_____________。
BaSO4(s) ΔH=_____________。
Ⅱ.SO2的尾气处理通常有以下几种方法:
(1)活性炭还原法
反应原理:恒温恒容时2C(s)+2SO2(g)![]() S2(g)+2CO2(g)。
S2(g)+2CO2(g)。
反应进行到不同时间测得各物质的浓度部分图象如图:
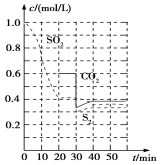
①0~20 min反应速率表示为v(SO2)=________;
②30 min时,改变某一条件平衡发生移动,则改变的条件最有可能是________;
③40 min时,平衡常数K=________。
(2)亚硫酸钠吸收法
①Na2SO3溶液吸收SO2的离子方程式为__________________;
②常温下,当吸收至NaHSO3时,吸收液中相关离子浓度关系一定正确的是________(填序号)。
a.c(Na+)+c(H+)>c(![]() )+c(
)+c(![]() )+c(OH)
)+c(OH)
b.水电离出c(H+)=1×108 mol/L
c.c(Na+)>c(![]() )>c(H+)>c(
)>c(H+)>c(![]() )
)
(3)电化学处理法

①如图所示,Pt(Ⅰ)电极的反应式为__________________;
②当电路中转移0.02 mol e时(较浓H2SO4尚未排出),交换膜左侧溶液中约增加____mol离子。
【答案】Ⅰ.1473.2 kJ·mol1
Ⅱ.(1)①0.03 mol/(L·min) ②减少CO2的浓度 ③0.675
(2)①![]() +SO2+H2O
+SO2+H2O![]() 2
2![]() ②ac
②ac
(3)①SO22e+2H2O![]()
![]() +4H+ ②0.03
+4H+ ②0.03
【解析】Ⅰ.已知:①BaSO4(s) +4C(s) ![]() BaS(s) +4CO(g) ΔH=+571.2 kJ·mol1
BaS(s) +4CO(g) ΔH=+571.2 kJ·mol1
②BaS(s) ![]() Ba(s)+S(s) ΔH=+460 kJ·mol1
Ba(s)+S(s) ΔH=+460 kJ·mol1
③2C(s)+O2(g) ![]() 2CO(g) ΔH=221 kJ·mol1,根据盖斯定律分析,反应③×2反应①反应②可得热化学方程式为Ba(s)+S(s)+2O2(g)
2CO(g) ΔH=221 kJ·mol1,根据盖斯定律分析,反应③×2反应①反应②可得热化学方程式为Ba(s)+S(s)+2O2(g) ![]() BaSO4(s) ΔH=221 kJ·mol1×2460 kJ·mol1571.2 kJ·mol1=
BaSO4(s) ΔH=221 kJ·mol1×2460 kJ·mol1571.2 kJ·mol1=
1473.2 kJ·mol1。
Ⅱ.(1)①由图可知,0~20分钟内二氧化硫浓度变化量为1 mol/L0.4 mol/L=0.6 mol/L,故二氧化硫的反应速率=0.6 mol/L÷20 min=0.03 mol/(L·min)。
②30分钟时瞬间,二氧化碳的浓度降低,S2的浓度不变,而后二氧化碳和S2的浓度均增大,应是减小二氧化碳的浓度。
③其平衡常数为生成物的浓度幂之积/反应物浓度的幂之积,由于平衡常数只与温度有关系,则K=![]() =
=![]() =0.675。
=0.675。
(2)①亚硫酸钠溶液与二氧化硫反应生成亚硫酸氢钠,反应离子方程式为![]() +SO2+H2O
+SO2+H2O![]() 2
2![]() 。
。
②a.根据电荷守恒,c(Na+)+c(H+)=2c(![]() )+c(
)+c(![]() )+c(OH),所以c(Na+)+c(H+)>c(
)+c(OH),所以c(Na+)+c(H+)>c(![]() )+c(
)+c(![]() )+
)+
c(OH),a正确。b.水电离出的氢离子浓度等于水电离出的氢氧根离子浓度,由于亚硫酸氢钠溶液的pH未知,所以不能计算水电离出c(H+)浓度,b错误。c.在亚硫酸氢钠溶液中亚硫酸氢根的电离大于水解,所以离子浓度关系为c(Na+)>c(![]() )>c(H+)>c(
)>c(H+)>c(![]() ),c正确。所以选ac。
),c正确。所以选ac。
(3)①由图可知,Pt(Ⅰ)电极上二氧化硫氧化成硫酸,电极反应为SO22e+2H2O![]()
![]() +4H+。
+4H+。
②左侧电解反应SO22e+2H2O![]()
![]() +4H+,根据电子守恒,生成硫酸根的物质的量为0.02 mol/2=0.01 mol,生成氢离子物质的量为0.04 mol,为保持溶液电中性,0.01 mol的硫酸根需要0.02 mol的氢离子,多余的氢离子通过阳离子交换膜移动到右侧,即有0.02 mol氢离子移动到右侧,故左侧溶液中增加的离子为0.01 mol+0.02 mol=0.03 mol。
+4H+,根据电子守恒,生成硫酸根的物质的量为0.02 mol/2=0.01 mol,生成氢离子物质的量为0.04 mol,为保持溶液电中性,0.01 mol的硫酸根需要0.02 mol的氢离子,多余的氢离子通过阳离子交换膜移动到右侧,即有0.02 mol氢离子移动到右侧,故左侧溶液中增加的离子为0.01 mol+0.02 mol=0.03 mol。

 期末集结号系列答案
期末集结号系列答案【题目】POC13常用作半导体掺杂剂及光导纤维原料,实验室制备POC13并测定产品含量的实验过程如下:
I.实验室制备POC13。
采用氧气氧化液态PCl3法制取POC13,实验装置(加热及夹持仪器略)如图:

资料:①Ag+SCN-==AgSCN↓:Ksp(AgCl)>Ksp(AgSCN);
②PCl3和POC13的相关信息如下表:
物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
PCl3 | -112.0 | 76.0 | 137.5 | 两者互溶,均为无色液体,遇水均剧烈反应生成含氧酸和氯化氢 |
POC13 | 2.0 | 106.0 | 153.5 |
(1)B中所盛的试剂是________,干燥管的作用是_____________________。
(2)POC13遇水反应的化学方程式为____________________________。
(3)装置B的作用除干燥O2外,还有_____________________________。
(4)反应温度要控制在60~65℃,原因是:____________________________。
II.测定POC13产品的含量。
实验步骤:
①制备POC13实验结束后,待三颈瓶中的液体冷却至室温,准确称取30.7g POC13产品,置于盛有60.00 mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100. 00 mL溶液。
②取10. 00 mL溶液于锥形瓶中,加入10.00 mL 3.2mol/L AgNO3标准溶液。
③加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
④以X为指示剂,用0.2 mol/L KSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去l0.00 mLKSCN溶液。
(5)步骤③中加入硝基苯的作用是__________________________。
(6)步骤④中X为____________________ 。
(7)反应中POC13的百分含量为_________,通过__________(填操作)可以提高产品的纯度。