题目内容
【题目】50mL 0.50molL﹣1盐酸与50mL 0.55molL﹣1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
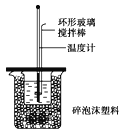
(1)大小烧杯间填满碎纸条的作用是______;
(2)大烧杯上如不盖硬纸板,求得的中和热数值将___(填“偏大”、“偏小”或“无影响”),结合日常生活的实际该实验在____进行效果更好;
(3)实验中改用60mL0.50molL﹣1盐酸与50mL0.55molL﹣1NaOH溶液进行反应,与上述实验相比,所放出的热量______(填“相等”、“不相等”),简述理由:_____;
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会_____;用50mL 0.5mo1L﹣1NaOH溶液进行上述实验,测得的中和热的数值会____(填“偏大”、“偏小”或“无影响”)
【答案】减少实验过程中的热量损失 偏小 保温杯 不相等 反应放出的热量和所用酸以及碱的量的多少有关 偏小 无影响
【解析】
本题考查的是中和热的测定。
(1)中和热测定实验成败的关键是保温工作;
(2)大烧杯上如不盖硬纸板,会使一部分热量散失;日常生活中我们经常用到保温杯,在保温杯中进行实验保温效果会更好;
(3)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;(4)根据弱电解质电离吸热分析;根据中和热的概念分析。据此解答。
(1)中和热测定实验成败的关键是保温措施,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失。本小题答案为:减少实验过程中的热量损失。
(2)大烧杯上如不盖硬纸板,会使一部分热量散失,求得的中和热数值将会减小;在日常生活实际该实验在保温杯中效果更好。本小题答案为:偏小;保温杯。
(3)反应放出的热量和所用酸以及碱的量的多少有关,用60mL 0.50molL1盐酸与50mL 0.55molL1NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量增多。本小题答案为:不相等;反应放出的热量和所用酸以及碱的量的多少有关。
(4)氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量偏少,中和热的数值会偏小;
中和热指的是强酸和强碱在稀溶液中反应生成1mol水时放出的热量,与酸碱的用量无关,所以用5mL0.50mol/LNaOH溶液进行上述实验,对测得的中和热的数值无影响。本小题答案为:偏小;无影响。

 阅读快车系列答案
阅读快车系列答案