题目内容
一定条件下,将A、B、C三种物质各1 mol通入一个密闭容器中发生反应:2A+B 2C,达到化学反应限度时,B的物质的量可能是( )。
2C,达到化学反应限度时,B的物质的量可能是( )。
A.1.5 mol B.1 mol C.0.5 mol D.0
B
解析

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
下列反应中,同时符合图像Ⅰ和Ⅱ的是
A.N2(g)+3H2(g) 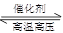 2NH3(g) ΔH<0 2NH3(g) ΔH<0 |
B.2SO3(g)  2SO2(g)+O2(g) ΔH>0 2SO2(g)+O2(g) ΔH>0 |
C.H2(g)+CO(g)  C(s)+H2O(g) ΔH>0 C(s)+H2O(g) ΔH>0 |
D.4NH3(g)+5O2(g)  4NO(g)+6H2O(g) ΔH<0 4NO(g)+6H2O(g) ΔH<0 |
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s)  NH3(g) + HI(g) ②2HI(g)
NH3(g) + HI(g) ②2HI(g)  H2(g) + I2(g)
H2(g) + I2(g)
达到平衡时,c(H2)=0.5mol/L,c(NH3)=4mol/L,则此温度下反应①的平衡常数为
| A.9 | B.12 | C.16 | D.20 |
下列有关化学反应速率的说法不正确的是( )
| A.化学反应达到最大限度时,正逆反应速率也达到最大且相等 |
| B.催化剂能降低化学反应的活化能,加快反应速率,提高生产效率 |
| C.用锌和稀硫酸反应制取H2时,滴加几滴硫酸铜溶液能加快反应速率 |
| D.用铁片和稀硫酸反应制H2比用98%的浓硫酸产生H2的速率快 |
反应2SO2+O2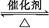 2SO3经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·(L·s)-1,则这段时间为( )
2SO3经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·(L·s)-1,则这段时间为( )
| A.0.1 s | B.2.5 s | C.10 s | D.5 s |
一定温度下,体积为2 L的密闭容器中X、Y、Z三种气体的初始物质的量和平衡物质的量如下表:
| 物质 | X | Y | Z |
| 初始物质的量(mol) | 0.2 | 0.2 | 0 |
| 平衡物质的量(mol) | 0.1 | 0.05 | 0.1 |
下列说法正确的是( )
A.反应可表示为2X+3Y
 2Z,其平衡常数为8 000
2Z,其平衡常数为8 000B.增大压强使平衡向生成Z的方向移动,平衡常数增大
C.若将容器的体积压缩至1 L,则X的体积分数减小,浓度增大
D.若升高温度时,Z的浓度增大,可知温度升高时正反应速率增大,逆反应速率减小,平衡向正反应方向移动
用铁片和稀硫酸反应制取H2时,下列措施不能使氢气的生成速率增大的是( )。
| A.加热 |
| B.不用稀硫酸,而改用98%的浓硫酸 |
| C.滴加少量浓盐酸 |
| D.不用铁片,改用铁粉 |
在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个带有理想活塞(即无质量、无摩擦力的刚性活塞)的体积可变的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g) A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是( )
A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是( )
| A.平衡时C的转化率:乙>甲 |
| B.平衡时C的体积分数:乙>甲 |
| C.反应速率:乙>甲 |
| D.平衡时A的物质的量:甲>乙 |
 pC(g)+qD中,A和C都是无色气体,达到平衡后,下列叙述正确的是 ( )。
pC(g)+qD中,A和C都是无色气体,达到平衡后,下列叙述正确的是 ( )。