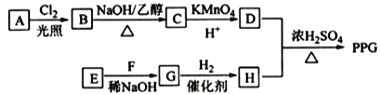
题目内容
【题目】已知用硫酸酸化的草酸(H2C2O4)溶液能与KMnO4溶液反应.某化学小组研究发现,少量MnSO4可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下:
(1)常温下,探究不同的初始pH和草酸溶液浓度对反应速率的影响,设计如下实验,则A= , C= , E=
实验编号 | 温度 | 初始pH | 0.1mol/L草酸溶液体积/mL | 0.01mol/LKMnO4 | 蒸馏水体积/mL | 待测数据(混合液褪色时间/s) |
① | 常温 | 1 | 20 | 50 | 30 | t1 |
② | 常温 | A | B | C | 30 | t2 |
③ | 常温 | 2 | 40 | D | E | t3 |
(2)该反应的离子方程式 .
(3)若t1<t2 , 则根据实验①和②得到的结论是 .
(4)小组同学发现每组实验反应速率随时间的变化总是如图,其中t1~t2时间内速率变快的主要原因可能是: 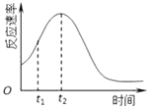
①;②
(5)化学小组用滴定法测定KMnO4溶液物质的量浓度:取ag草酸晶体(H2C2O42H2O,摩尔质量126g/mol)溶于水配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入适量稀H2SO4酸化,再用KMnO4溶液滴定至终点,重复滴定三次,平均消耗KMnO4溶液VmL.滴定到达终点的现象是:;实验中所需的定量仪器有(填仪器名称).该KMnO4溶液的物质的量浓度为mol/L.
【答案】
(1)2;50;10
(2)5H2C2O4+2MnO4﹣+6H+=10CO2+2Mn2++8H2O
(3)其他条件相同时,溶液的初始pH越小,该反应的反应速率越快
(4)该反应放热;产物Mn2+是反应的催化剂
(5)滴入最后一滴KMnO4溶液,溶液呈浅紫红色,且30秒内不恢复;托盘天平、250mL容量瓶、酸式滴定管;![]()
【解析】解:(1)根据该实验探究不同的初始pH和草酸溶液浓度对反应速率的影响,实验要求控制KMnO4溶液初始浓度相同,则KMnO4溶液的体积为50mL,总体积为100mL,则C=50,D=50,B=20,E=10,探究外界条件对反应速率的影响,需保证其他条件相同,则①与②的pH不同,②与③的草酸浓度不同,
则A=2,
故答案为:2;50;10;(2)草酸与高锰酸钾反应是锰离子和二氧化碳、水,其反应的离子方程式为:5H2C2O4+2MnO4﹣+6H+=10CO2↑+2Mn2++8H2O;
故答案为:5H2C2O4+2MnO4﹣+6H+=10CO2↑+2Mn2++8H2O;(3)实验①和②只有pH不同,其它条件都相同,而且t1<t2 , 说明其他条件相同时,溶液的初始pH越小,该反应的反应速率越快;
故答案为:其他条件相同时,溶液的初始pH越小,该反应的反应速率越快;(4)对于该反应,影响化学反应的速率只有温度和催化剂,所以反应速率随时间的变化总是如图,其中t1~t2时间内速率变快的主要原因可能是:反应放热,温度升高或产物Mn2+是反应的催化剂;
故答案为:该反应放热;产物Mn2+是反应的催化剂;(5)高锰酸钾本身有颜色,故不需要另加指示剂,草酸反应完毕,加入最后一滴KMnO4溶液,溶液变为红色,红色30s内不褪去,说明滴定到终点;
称量固体用托盘天平、配制250ml溶液用250mL容量瓶、量取KMnO4溶液和草酸溶液用到酸式滴定管;
c(草酸)= ![]() =
= ![]() mol/L
mol/L
由关系式
2KMnO4 | ~ | 5H2C2O4 |
2 | 5 | |
cmolL﹣1×V×10﹣3L |
|
c= ![]() mol/L=
mol/L= ![]() mol/L,
mol/L,
故答案为:加入最后一滴KMnO4溶液,溶液变为红色,且30s内红色不褪去;托盘天平、250mL容量瓶、(酸式)滴定管; ![]() ;
;
(1)根据该实验探究不同的初始pH和草酸溶液浓度对反应速率的影响,所以KMnO4的浓度不变,探究外界条件对反应速率的影响,需保证其他条件相同时来实验;(2)草酸与高锰酸钾反应是锰离子和二氧化碳、水;(3)实验①和②只有pH不同,其它条件都相同;(4)根据外界条件对化学反应速率的影响;(5)草酸反应完毕,加入最后一滴KMnO4溶液,溶液变为红色,红色30s内不褪去,说明滴定到终点;
根据称量固体用天平、配制溶液用容量瓶、量取液体用滴定管分析;
先求出醋酸的浓度,再由关系式2KMnO4~5H2C2O4计算.

 全能测控一本好卷系列答案
全能测控一本好卷系列答案【题目】煤的气化是高效、清洁的利用煤炭的重要途径之一.
(1)焦炭与水蒸气反应是将固体煤变为气体燃料的方法.已知:
①C(s)+O2 (g)=CO2 (g)△H=﹣393.5kJmol﹣1
②CO(g)+ ![]() O2 (g)=CO2 (g)△H=﹣283.0kJmol﹣1
O2 (g)=CO2 (g)△H=﹣283.0kJmol﹣1
③H2(g)+ ![]() O2 (g)=H2O (g)△H=﹣241.8kJmol﹣1
O2 (g)=H2O (g)△H=﹣241.8kJmol﹣1
则碳与水蒸气反应生成一氧化碳和氢气的热化学方程式是 , 该反应的化学平衡常数K随温度的升高将(填“增大”、“减小”或“不变”).
(2)CO可以与H2O(g)进一步发生反应CO(g)+H2O(g)CO2(g)+H2(g)△H<0.在甲、乙两个恒容密闭容器中,起始时按照表数据进行投料,在800℃时达到平衡状态,K=1.0.
H2O | CO | CO2 | H2 | |
甲 n/mol | 0.10 | 0.30 | 0.10 | 0.50 |
乙 n/mol | 0.20 | 0.20 | 0 | 0 |
起始时,甲容器中反应向(填“正反应”或“逆反应”)方向进行;平衡时,乙容器中CO的转化率为 .
(3)以CO为燃料制作燃料电池,电池的正极通入O2和CO2 , 负极通入CO,电解质是熔融碳酸钠,写出工作时正极的电极反应式: , 若使用该电池电解熔融Al2O3制取10.8g Al,则理论上需要氧气的体积为(标准状况下)L.
(4)将(2)中生成的混合气用过量的NaOH溶液吸收,得到的溶液中有一种溶质可以水解,请写出其水解的离子方程式: , .