题目内容
Na2O2是常见的氧化钠,某化学小组的同学欲通过以下实验确定炭粉与Na2O2的反应产物。
【实验步骤】
Ⅰ.按如图所示装置(部分仪器未画出)组装仪器,并检查装置气密性。
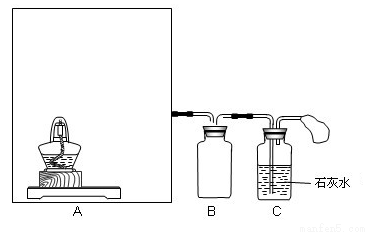
Ⅱ.将0.6g炭粉与3.9gNa2O2均匀混合,装入A装置中的反应容器,在靠近试管口处放置一张湿润的氯化钯试纸(湿润氯化钯试纸CO变黑,可用于检验是否有CO生成)。
Ⅲ.用酒精灯微微加热A装置中的反应容器
【实验现象】
试管中发生剧烈反应并产生火花,氯化钯试纸未变黑,石灰水未变浑浊。
回答下列问题:
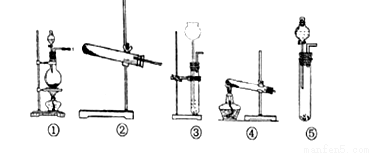
(1)在A装置中方框内的仪器可以选用_____________(①②③④⑤中选出所需的装置,使仪器装置图完整)。
(2)装置B的作用是________________。
(3)通过探究发现,装置A中只发生反应2Na2O2+C Na2CO3+X,则X为___________(填化学式)。
Na2CO3+X,则X为___________(填化学式)。
(4)CO在潮湿环境中可将氯化钯还原为黑色粉末状的钯(Pd),同时生成另外两种新物质.已知反应过程中转移6.02×1023个电子时,生成53g Pd,该反应的化学方程式为________________________。
(5)将装置A中完全反应后所得物质溶于适量水,配成溶液,回答下列问题:
①所得溶液的溶质是___________(填化学式)。
②常温,若使所得溶液与100 mL稀盐酸恰好完全反应至溶液pH=7,该盐酸的物质的量浓度为___________。
(6)写出Na2O2的一种重要用途_________________。
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g) 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示:

容器 | 甲 | 乙 | 丙 |
容积 | 0.5 L | 0.5 L | 1.0 L |
温度/℃ | T1 | T2 | T2 |
反应物 起始量 | 1.5 mol A 0.5 mol B | 1.5 mol A 0.5 mol B | 6.0 mol A 2.0 mol B |
下列说法正确的是( )
A.平衡后,向甲容器中再充入0.5 mol A,A和B的转化率均增大
B.达到平衡时反应吸收的热量:Q丙> 2Q乙
C.若平衡时保持温度不变,改变容器体积平衡不移动
D.T1℃,起始时甲容器中充入0.5 mol A、1.5 mol B,平衡时A的转化率为25%


 有特殊香味的物质,该物质为_____________(填名称)。
有特殊香味的物质,该物质为_____________(填名称)。 碱
碱
 mol·L-1 C.0.25 mol·L-1 D.0.20 mol·L-1
mol·L-1 C.0.25 mol·L-1 D.0.20 mol·L-1