题目内容
氢氧燃料电池是一种用氢气作为能源的电池.这种燃料电池的效率要比传统内燃机的效率高很多,所以燃料电池汽车(FCV)会有很高的效率.Schlesinger等人提出可用NaBH4与水反应制氢气:BH4-+2H2O=BO2-+4H2↑(反应实质为水电离出来的H+被还原).该反应的产氢速率受外界条件影响.下表为pH和温度对NaBH4 半衰期的影响(半衰期是指反应过程中,某物质的浓度降低到初始浓度一半时所需的时间).
根据要求回答下列问题:
(1)已知,NaBH4与水反应后所得溶液显碱性,则溶液中各离子浓度大小关系为 .
(2)从上表可知,温度对NaBH4与水反应速率产生怎样的影响?答: .
(3)反应体系的pH为何会对NaBH4与水反应的反应速率产生影响?答: .
(4)实验表明,将NaBH4溶于足量水,释放的H2比理论产量少得多(即反应一段时间后有NaBH4剩余也不再反应).其可能原因是 .
| 体系 pH[ |
不同温度下NaBH4的半衰期(min) | |||
| 0℃ | 25℃ | 50℃ | 75℃ | |
| 8 | 4.32×100 | 6.19×10-1 | 8.64×10-2 | 1.22×10-2 |
| 10 | 4.32×102 | 6.19×101 | 8.64×100 | 1.22×100 |
| 12 | 4.32×104 | 6.19×103 | 8.64×102 | 1.22×102 |
| 14 | 4.32×106 | 6.19×105 | 8.64×104 | 1.22×104 |
(1)已知,NaBH4与水反应后所得溶液显碱性,则溶液中各离子浓度大小关系为
(2)从上表可知,温度对NaBH4与水反应速率产生怎样的影响?答:
(3)反应体系的pH为何会对NaBH4与水反应的反应速率产生影响?答:
(4)实验表明,将NaBH4溶于足量水,释放的H2比理论产量少得多(即反应一段时间后有NaBH4剩余也不再反应).其可能原因是
分析:(1)依据NaBH4与水反应制氢气:BH4-+2H2O=BO2-+4H2↑,反应生成的盐溶液BO2-在溶液中水解显碱性分析判断溶液中离子浓度大小;
(2)依据图表数据分析,随温度升高体系半衰期缩短,反应速率加快;
(3)分析图表数据可知PH增大,半衰期增长,反应速率减慢;
(4)随反应进行,溶液的pH逐渐增大,反应速率变小.常温时,当体系pH>12,半衰期为6. 19×103min分析反应速率变慢判断.
(2)依据图表数据分析,随温度升高体系半衰期缩短,反应速率加快;
(3)分析图表数据可知PH增大,半衰期增长,反应速率减慢;
(4)随反应进行,溶液的pH逐渐增大,反应速率变小.常温时,当体系pH>12,半衰期为6. 19×103min分析反应速率变慢判断.
解答:解:(1)NaBH4与水反应制氢气:BH4-+2H2O=BO2-+4H2↑,反应生成的盐溶液BO2-在溶液中水解显碱性,溶液中离子浓度大小为c(Na+)>c(BO2-)>c(OH-)>c(H+),
故答案为:c(Na+)>c(BO2-)>c(OH-)>c(H+);
(2)图表数据分析,随温度升高体系半衰期缩短,反应速率加快,故答案为:温度越大,反应速率越大;
(3)NaBH4与水反应制氢气:BH4-+2H2O=BO2-+4H2↑,反应实质为水电离出来的H+被还原,图表数据可知PH增大,半衰期增长,反应速率减慢,体系碱性越强,水电离出来的H+浓度越低,因而反应速率越慢,
故答案为:体系碱性越强,水电离出来的H+浓度越低,因而反应速率越慢;
(4)随反应进行,溶液的pH逐渐增大,反应速率变小.常温时,当体系pH>12,半衰期为6. 19×103min,反应速率很小,反应几乎停止,
故答案为:随反应进行,溶液的pH逐渐增大,反应速率变小.常温时,当体系pH>12,半衰期为6. 19×103min(约为4.3天),反应速率非常小,可认为反应停止.
故答案为:c(Na+)>c(BO2-)>c(OH-)>c(H+);
(2)图表数据分析,随温度升高体系半衰期缩短,反应速率加快,故答案为:温度越大,反应速率越大;
(3)NaBH4与水反应制氢气:BH4-+2H2O=BO2-+4H2↑,反应实质为水电离出来的H+被还原,图表数据可知PH增大,半衰期增长,反应速率减慢,体系碱性越强,水电离出来的H+浓度越低,因而反应速率越慢,
故答案为:体系碱性越强,水电离出来的H+浓度越低,因而反应速率越慢;
(4)随反应进行,溶液的pH逐渐增大,反应速率变小.常温时,当体系pH>12,半衰期为6. 19×103min,反应速率很小,反应几乎停止,
故答案为:随反应进行,溶液的pH逐渐增大,反应速率变小.常温时,当体系pH>12,半衰期为6. 19×103min(约为4.3天),反应速率非常小,可认为反应停止.
点评:本题考查了溶液碱性的原因和图表数据分析总结规律和分析应用判断,题干信息的应用和分析判断是解题关键,题目难度中等.

练习册系列答案
相关题目
 化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.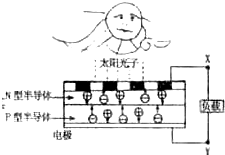
 英国国家海洋学中心于2009年8月14日发布新闻公报说,中心的研究人员及其同行利用声呐等手段探测到北极海洋中存在大量甲烷气泡,证实了全球变暖会使海底释放大量甲烷的说法。研究人员认为,这些甲烷可能会反过来加剧全球变暖。
英国国家海洋学中心于2009年8月14日发布新闻公报说,中心的研究人员及其同行利用声呐等手段探测到北极海洋中存在大量甲烷气泡,证实了全球变暖会使海底释放大量甲烷的说法。研究人员认为,这些甲烷可能会反过来加剧全球变暖。 (2)美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的电池,氢气虽然使用方便,却受到价格和来源的限制。常用的燃料往往是某些碳氢化合物,如甲烷(天然气)、汽油等。电池的构造如图所示:两个电极均由多孔碳制成,通入的气体由孔隙中流出,并从电极表面放出。
(2)美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的电池,氢气虽然使用方便,却受到价格和来源的限制。常用的燃料往往是某些碳氢化合物,如甲烷(天然气)、汽油等。电池的构造如图所示:两个电极均由多孔碳制成,通入的气体由孔隙中流出,并从电极表面放出。 (3)某课外活动小组利用右图所示装置探究甲烷于氯气的反应。根据题意,回答下列问题:
(3)某课外活动小组利用右图所示装置探究甲烷于氯气的反应。根据题意,回答下列问题: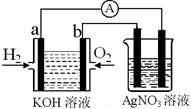
 2H2O
2H2O