题目内容
如下图为10 mL一定物质的量浓度的HCl溶液用一定物质的量浓度的NaOH溶液滴定的图示。请根据图示计算: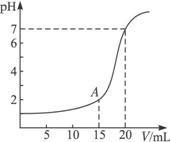
(1)氢氧化钠物质的量浓度是多少?
(2)A点时溶液的pH是多少?
解析:(1)根据题给图象可以看出,在氢氧化钠的体积为0时,盐酸溶液的pH=1,故可求出盐酸溶液的物质的量浓度为0.1 mol·L-1;再根据pH=7时,用去氢氧化钠的体积为20 mL,此时盐酸与氧氧化钠恰好完全反应,则有
(2)A点时,显然盐酸是过量的,则加入的氢氧化钠与盐酸反应后剩余的盐酸为
c(H+)=![]() =1×10-2 mol·L-1,所以,pH=2。
=1×10-2 mol·L-1,所以,pH=2。
答案:(1)0.05 mol·L-1 (2)2

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
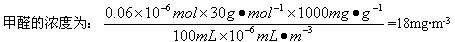
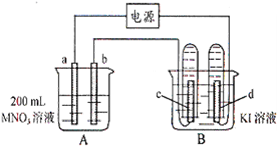
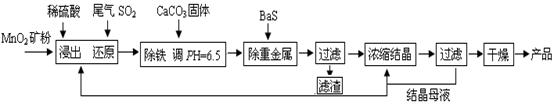
 的产物是Mn3O4、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是 ▲
的产物是Mn3O4、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是 ▲