题目内容
某课外活动小组用如图所示装置做炼铁原理的实验,同时检测氧化铁纯度。
CO气体用下列反应来制取:
H2C2O4![]() CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
乙二酸
(1)若所制气体从左向右流向时,将上述仪器组装连接的顺序是(用a,b,c,…表示)
![]() 接
接![]()
![]() 接
接![]()
![]() 接
接![]()
![]() 接
接![]()
(2)实验操作可分解为如下几步:
A.点燃甲装置中的酒精灯
B.检查装置的气密性
C.排净全套装置的空气
D.点燃乙装置中C导出的CO
E.点燃装置戊处的酒精灯
P.按实验要求将仪器连接好
G.待装置戊中的还原产物冷却至常温时,熄灭甲处的酒精灯
H.待装置戊中的氧化铁粉末变成黑色时,熄灭戊处的酒精灯
则正确操作的顺序是(填A,B,C,…)
![]() →
→![]() →
→![]() →C→
→C→![]() →
→![]() →
→![]() →
→![]() →
→
(3)简要回答:
装置乙的作用是________,装置丙的作用是_______,先熄灭戊处的酒精灯后才熄灭甲处的酒精灯,其主要原因是_________________________。
实验前,氧化铁粉末为x(g),实验后乙、丙的质量分别增加y(g)和z(g),则氧化铁的质量分数为_____________________________。
答案:
解析:
解析:
| (1)ae df gh i(或ih)b (2)F,B,A(C),D,E,H,G (3)吸收生成的CO2 除去未反应完的CO,防止污染空气 除去甲中生成的CO2,防止生成的铁在高温下被氧化;防止丙中溶液倒吸入甲中; (1)通入戊中的气体必为纯净干燥的CO (2)乙中增加的质量应为CO与Fe2O3反应生成CO2的质量。
|

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

 某课外活动小组用如图所示装置进行实验(电解液足量).下列说法正确的是( )
某课外活动小组用如图所示装置进行实验(电解液足量).下列说法正确的是( )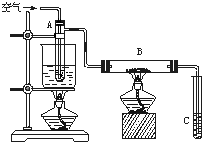 某课外活动小组用如图所示进行乙醇的催化氧化实验探究,试管A中盛有无水乙醇,B中装有CuO(用石棉绒作载体),试管C中放的是蒸馏水.请回答下列问题:
某课外活动小组用如图所示进行乙醇的催化氧化实验探究,试管A中盛有无水乙醇,B中装有CuO(用石棉绒作载体),试管C中放的是蒸馏水.请回答下列问题:

