题目内容
4.用NaOH固体配制1.0mol•L-1的NaOH溶液220mL,下列说法正确的是( )| A. | 首先称取NaOH固体8.8g | |
| B. | 容量瓶中原有少量蒸馏水没有影响 | |
| C. | 定容后,将容量瓶振荡均匀,静置时发现液面低于刻度线,于是又加少量水至刻度线 | |
| D. | 定容时仰视刻度线会使所配制的溶液浓度偏高 |
分析 配制1.0mol•L-1的NaOH溶液220mL,应选择250mL容量瓶,依据m=VCM计算溶质的质量;
分析不当操作对溶质的物质的量和溶液的体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:A.配制1.0mol•L-1的NaOH溶液220mL,应选择250mL容量瓶,需要氢氧化钠质量=1.0mol•L-1×0.25L×40g/mol=10.0g,故A错误;
B.容量瓶中原有少量蒸馏水,对溶质的物质的量和溶液的体积不会产生影响,溶液浓度不变,故B正确;
C.定容后,将容量瓶振荡均匀,静置时发现液面低于刻度线,于是又加少量水至刻度线,导致溶液体积偏大,溶液浓度偏小,故C错误;
D.定容时仰视刻度线会导致溶液体积偏大,溶液浓度偏低,故D错误;
故选:B.
点评 本题考查了一定物质的量浓度溶液的配制,熟悉配制原理是解题关键,注意容量瓶规格的选择,注意误差分析方法,题目难度不大.

练习册系列答案
相关题目
8.硫酸,亚硫酸和氢硫酸是含硫的三种酸,下列说法不正确的是( )
| A. | 若向Na2S溶液中通入SO2则产生淡黄色沉淀 | |
| B. | 这三种酸都是二元酸,都能与氢氧化钠反应生成酸式盐和正盐 | |
| C. | 这三种酸的水溶液久置空气中都会变质且原溶质的浓度减小 | |
| D. | 向氢硫酸,亚硫酸溶液中滴加氯水都会发生氧化还原反应 |
19.若a mol H2SO4中含有b个氧原子,则阿伏加德罗常数可表示为( )
| A. | $\frac{a}{4b}$mol-1 | B. | $\frac{4b}{a}$ mol-1 | C. | $\frac{a}{b}$ mol-1 | D. | $\frac{b}{4a}$ mol-1 |
9.二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命.二甘醇的结构简式是HO-CH2CH2-O-CH2CH2-OH.下列有关二甘醇的叙述正确的是( )
| A. | 不能发生消去反应 | B. | 能发生取代反应 | ||
| C. | 能溶于水,不溶于乙醇 | D. | 不能氧化为醛 |
16.将含有0.4molCuSO4和0.4molNaCl的水溶液1L,用惰性电极电解一段时间后,在一个电极上得到0.3mol铜,在另一电极上析出的气体在标准状况下的体积是( )
| A. | 5.6L | B. | 6.75L | C. | 13.44L | D. | 11.2L |
13.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1 mol•L-1的Na2CO3溶液:K+、Ba2+、NO3-、Cl- | |
| B. | 0.1 mol•L-1FeCl3溶液:K+、NH4+、I-、OH- | |
| C. | 8 mol•L-1HNO3的溶液:Fe2+、H+、Cl-、Na+ | |
| D. | 0.1 mol•L-1的NaOH溶液:K+、Na+、SO42-、CO32- |
14.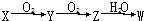 已知X、Y、Z、W(含同一元素)有如图所示的转化关系,若X是一种单质,W为一种含氧酸,则X不可能是( )
已知X、Y、Z、W(含同一元素)有如图所示的转化关系,若X是一种单质,W为一种含氧酸,则X不可能是( )
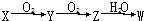 已知X、Y、Z、W(含同一元素)有如图所示的转化关系,若X是一种单质,W为一种含氧酸,则X不可能是( )
已知X、Y、Z、W(含同一元素)有如图所示的转化关系,若X是一种单质,W为一种含氧酸,则X不可能是( )| A. | N2 | B. | C | C. | S | D. | Si |
 .
. .
.