题目内容
15.在四种不同反应条件下,反应A(g)+B(g)=2C(g)+2D(g)的反应速率如下,其中反应最快的是( )| A. | V(A)=0.15 mol•L-1•S-1 | B. | V(B)=0.3 mol•L-1•S-1 | ||
| C. | V(C)=0.4 mol•L-1•S-1 | D. | V(D)=0.45 mol•L-1•S-1 |
分析 根据不同物质表示的速率之比等于其化学计量数之比,都转化为同一物质表示的速率,然后进行比较.
解答 解:对于反应:A(g)+B(g)═2C(g)+2D(g),都转化C表示的速率进行比较,
A.v(A)=0.15 mol•L-1•S-1,则v(C)=2v(A)=0.3 mol•L-1•S-1;
B.v(B)=0.3 mol•L-1•S-1,则v(C)=2v(B)=0.6 mol•L-1•S-1;
C.v(C)=0.4mol•L-1•S-1;
D.v(D)=0.45 mol•L-1•S-1,则v(C)=v(D)=0.45 mol•L-1•S-1,
故反应速率v(B)>v(D)>v(C)>v(A),
故选B.
点评 本题考查反应速率的比较,也可以利用反应速率与化学计量数的比值判断,比值越大反应速率越快,题目难度不大.

练习册系列答案
相关题目
5.下列有关氢化物的叙述中正确的是( )
| A. | 稳定性:H2S>HF | B. | HCl的电子式为 | ||
| C. | H2O的摩尔质量为18 | D. | 在卤化氢中HI最稳定 |
6.下列情况不能用胶体知识加以解释的是( )
| A. | 氯化铝溶液中加入小苏打溶液会产生白色沉淀和无色气体 | |
| B. | 肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 | |
| C. | 水泥厂、冶金厂常用高压电除工厂烟尘,以减少对空气的污染 | |
| D. | 牛油与烧碱溶液共热,向反应所得溶液中加入食盐,则有固体析出 |
3.0.1mol•L-1 KHS溶液中pH=11,下列表达式不正确的是( )
| A. | c(K +)+c(H+)=c(OH-)+c(HS-)+2 c(S2-) | B. | c(K+)>c(HS-)>c(OH-)>c(H+)>c(S2-) | ||
| C. | c(HS-)+c(S2-)+c(H2S)=0.1 mol•L-1 | D. | c(OH-)=2c(H2S)+c(H+)+c(HS-) |
10.如图与金属腐蚀有关的说法,正确的是( )
| A. | 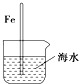 插入海水中的铁棒,越靠近底端腐蚀越严重 | |
| B. | 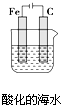 插入溶液中的铁棒容易溶解,主要是发生电化学腐蚀 | |
| C. |  燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀 | |
| D. | 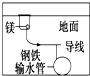 用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的阴极 |
5.下列有关实验的做法错误的是( )
| A. | 除去铁粉中混有的少量铝粉,可加人过量的氢氧化钠溶液,完全反应后过滤 | |
| B. | 除去FeCl2溶液中少量的FeCl3,可加入过量的铁粉,完全反应后过滤 | |
| C. | 用渗析的方法可除去Fe(OH)3胶体中混有的Cl- | |
| D. | 加入适量的NaOH可除去NaHCO3溶液中混有的少量Na2CO3 |

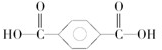 和
和 .
.
 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$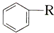 +HCl
+HCl
 .
. .
.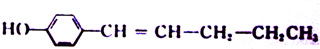 .
.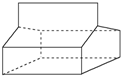 完成下列各小题.
完成下列各小题.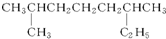 系统命名:2,6二甲基辛烷;
系统命名:2,6二甲基辛烷; ;
;