题目内容
【题目】50mL 0.50molL﹣1盐酸与50mL 0.55molL﹣1NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.试回答下列问题: 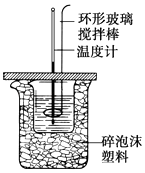
(1)大烧杯上如不盖硬纸板,求得的中和热数值将(填“偏大”、“偏小”或“无影响”).结合日常生活的实际该实验在中进行效果更好.
(2)实验中改用60m L 0.50molL﹣1盐酸与 50m L 0.55molL﹣1 NaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等”或“不相等”),所求中和热(填“相等”或“不相等”),简述理由 .
(3)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会;用50m L 0.5molL﹣1 NaOH溶液进行上述实验,测得的中和热的数值会 . (均填“偏大”、“偏小”或“无影响”)
【答案】
(1)偏小;保温杯
(2)不相等;相等;中和热是在稀溶液中,1molH+和1molOH﹣发生中和反应生成1molH2O时所放出的热量,与酸碱的用量无关
(3)偏小;偏小
【解析】解:(1)如不盖硬纸板,热量散失,不能准确测定最高温度,则求得的中和热数值将偏小,结合日常生活的实际该实验在保温杯中进行效果更好,
所以答案是:偏小;保温杯;(2)改用60m L 0.50molL﹣1盐酸与 50m L 0.55molL﹣1 NaOH溶液进行反应,生成水更多,放出的热量对,但中和热不变,因中和热是在稀溶液中,1 mol H+和1 mol OH﹣发生中和反应生成1 mol H2O时所放出的热量,与酸碱的用量无关,
所以答案是:不相等;相等;因中和热是在稀溶液中,1 mol H+和1 mol OH﹣发生中和反应生成1 mol H2O时所放出的热量,与酸碱的用量无关;(3)一水合氨电离吸热,则用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会偏小;用50m L 0.5molL﹣1 NaOH溶液进行上述实验,HCl不能完全反应,测得的中和热的数值会偏小,所以答案是:偏小;偏小.

 同步练习强化拓展系列答案
同步练习强化拓展系列答案