题目内容
【题目】已知A为淡黄色固体,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀。

(1)物质A的化学式为 ________。
(2)H在潮湿空气中变成M的实验现象是______________________________________,化学方程式为___________________________________________。
(3)A和水反应生成B和C的离子方程式为___________________________________,由此反应可知A有作为_________的用途。
(4)步骤①的离子方程式_______________________________________,请写出检验步骤①得到的溶液中主要阳离子(除H+外)所需要的试剂:_____________、____________(填化学式)。
【答案】Na2O2 白色沉淀迅速变为灰绿色,最终变为红褐色 4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3 2Na2O2 + 2H2O = 4Na+ + 4OH- + O2↑ 供氧剂 Fe3O4+8H+ = Fe2++2Fe3+ + 4H2O KSCN K3[Fe(CN)6]
【解析】
已知A为淡黄色固体,能与水反应生成B和C,A为Na2O2,与水反应生成NaOH和O2,C为气体,则C为O2、B为NaOH,T为生活中使用最广泛的金属单质,T为Fe,Fe能与O2在点燃时反应生成D为Fe3O4,Fe3O4先与盐酸反应生成FeCl2、FeCl3和水,再加入足量铁粉,Fe与Fe3+反应生成Fe2+,则E为FeCl2,FeCl2与NaOH溶液反应生成H为Fe(OH)2,Fe(OH)2在潮湿的空气中与氧气反应生成M为Fe(OH)3。
(1). 由上述分析可知,A为过氧化钠,化学式为Na2O2,故答案为:Na2O2;
(2). Fe(OH)2在潮湿的空气中与氧气反应生成M为Fe(OH)3,实验现象是白色沉淀迅速变为灰绿色,最终变为红褐色,化学反应方程式为4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3,故答案为:白色沉淀迅速变为灰绿色,最终变为红褐色;4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3;
(3). 过氧化钠与水反应生成氢氧化钠和氧气,离子方程式为2Na2O2 + 2H2O = 4Na++ 4OH- + O2↑,由此反应可知Na2O2可以用作供氧剂,故答案为:2Na2O2 + 2H2O = 4Na++ 4OH- + O2↑;供氧剂;
(4). Fe3O4与盐酸反应生成FeCl2、FeCl3和水,离子方程式为Fe3O4+8H+ = Fe2++2Fe3+ + 4H2O,①所得到的溶液中主要阳离子除H+外,还含有Fe2+、Fe3+,可选用KSCN检验Fe3+,用K3[Fe(CN)6]检验Fe2+,故答案为:KSCN;K3[Fe(CN)6]。

【题目】POC13常用作半导体掺杂剂及光导纤维原料,实验室制备POC13并测定产品含量的实验过程如下:
I.实验室制备POC13。
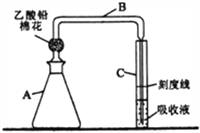
采用氧气氧化液态PCl3法制取POC13,实验装置(加热及夹持仪器略)如图:

资料:①Ag+SCN-==AgSCN↓:Ksp(AgCl)>Ksp(AgSCN);
②PCl3和POC13的相关信息如下表:
物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
PCl3 | -112.0 | 76.0 | 137.5 | 两者互溶,均为无色液体,遇水均剧烈反应生成含氧酸和氯化氢 |
POC13 | 2.0 | 106.0 | 153.5 |
(1)B中所盛的试剂是________,干燥管的作用是_____________________。
(2)POC13遇水反应的化学方程式为____________________________。
(3)装置B的作用除干燥O2外,还有_____________________________。
(4)反应温度要控制在60~65℃,原因是:____________________________。
II.测定POC13产品的含量。
实验步骤:
①制备POC13实验结束后,待三颈瓶中的液体冷却至室温,准确称取30.7g POC13产品,置于盛有60.00 mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100. 00 mL溶液。
②取10. 00 mL溶液于锥形瓶中,加入10.00 mL 3.2mol/L AgNO3标准溶液。
③加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
④以X为指示剂,用0.2 mol/L KSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去l0.00 mLKSCN溶液。
(5)步骤③中加入硝基苯的作用是__________________________。
(6)步骤④中X为____________________ 。
(7)反应中POC13的百分含量为_________,通过__________(填操作)可以提高产品的纯度。