题目内容
下列实验中,操作和现象以及对应结论都正确且现象与结论具有因果关系的是( )
序号 | 操作和现象 | 结论 |
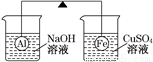
A | 取少量BaSO4固体于试管中,加入足量的盐酸,沉淀不溶解。 | BaSO4不溶于盐酸,且可以用盐酸 和BaCl2溶液检验SO42- |
B | 往乙醇中加入适量浓硫酸制备乙烯, | 证明乙烯能被酸性高锰酸钾氧化 |
C | 常温下,测得饱和NaA溶液的pH大于饱和NaB溶液 | 常温下水解程度:A﹣>B﹣ |
D | 在分液漏斗中加入碘水后再加入CCl4,充分振荡,分层,且上层溶液呈紫色 | CCl4可作为碘的萃取剂 |
A. A B. B C. C D. D
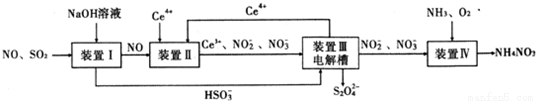
用HNO3和HF的混酸处理某金属后,产生的酸洗废液中含有Fe3+、Ni2+、NO3-、F-和Cr2O72-等。下图是综合利用该酸洗废液的工艺流程:
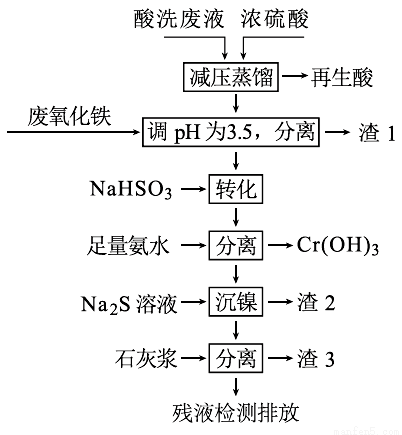
已知:
金属离子开始沉淀和沉淀完全时的pH:
Fe3+ | Ni2+ | Cr3+ | |
开始沉淀 | 1.5 | 6.7 | 4.0 |
沉淀完全 | 3.4 | 9.5 | 6.9 |
②Ni2+与足量氨水的反应为:Ni2++6NH3 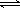 [Ni(NH3)6]2+
[Ni(NH3)6]2+
(1)再生酸中含有HNO3,采取减压蒸馏的目的为____________,
(2)滤渣1的主要成份为:____________。
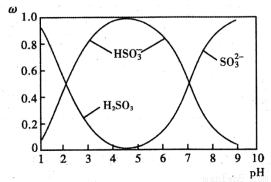
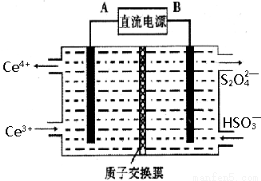
(3)请写出“转化”时NaHSO3与Cr2O72-发生反应的氧化剂与还原剂的物质的量之比:________。
(4)已知[Ni(NH3)6]2+为难电离的络合离子,则“沉镍”的离子方程式为:____________。
(5)滤渣3的主要成分为CaSO4、Ca(OH)2和_____。
(6)经检测,最后的残液中c(Ca2+)=0.001 mol•L-1,则残液中F-浓度为____mg•L-1,______(填“符合”或“不符合”)排放标准[已知Ksp(CaF2)=4×10-11,国家排放标准要求氟离子浓度小于10 mg•L-1]。
 并将产生的气体直接通入酸性高锰酸钾溶液中,溶液紫红
并将产生的气体直接通入酸性高锰酸钾溶液中,溶液紫红 色褪去
色褪去