题目内容
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1 mol/L氯化铜溶液中的Cu2+数小于NA |
| B.标准状况下,22.4 L Cl2参加任何化学反应转移的电子数都是2NA |
| C.28 g聚乙烯含有的碳原子数为2NA |
| D.1 mol CH5+所含电子数为8NA |
C
解析试题分析:A、1 mol/L氯化铜溶液中的Cu2+数无法计算,缺少体积,错误;B、氯气和水反应中氯气自身既做氧化剂,又做还原剂,1摩尔氯气转移1摩尔电子,错误;C、聚乙烯的摩尔质量为28ng/mol,含有2n个碳原子,因此碳原子数为28÷28n×2n×NA ="2" NA;正确;D、1 mol CH5+所含电子数为10 NA,错误。
考点:考查阿伏伽德罗常数的计算

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
NA表示阿伏加德罗常数的值。下列说法中,正确的是
| A.在反应KIO3+6HI=KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6NA |
| B.电解精炼铜时,当电路中转移NA个电子,阳极溶解32 g铜 |
| C.向仅含0.2 mol FeI2的溶液中持续通入氯气,当有0.1 mol Fe2+被氧化时,转移电子的数目为0.5NA |
| D.将100 mL 0.1 mol·L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA |
NA表示表示阿伏伽德罗常数的值,下列说法正确的是
| A.1mol Na2O2粉末中含离子总数为4NA |
| B.22.4LCO2中含有的原子数为3NA |
| C.1mol单质钠在常温下或点燃条件下与O2完全反应转移的电子数都为NA |
| D.在一定量的稀硝酸中加入56g铁粉且完全溶解,转移的电子一定为3NA |
设阿伏加德罗常数的数值为NA,下列说法正确的是
A.80mL 10mol 浓盐酸与足量MnO2反应,转移电子数为0.4NA 浓盐酸与足量MnO2反应,转移电子数为0.4NA |
| B.标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为2NA |
| C.1 mol A13+含有核外电子数为3NA |
| D.常温下,16g CH4中共用电子对的数目为4NA |
同温同压下,x g的甲气体和y g的乙气体占有相同的体积,根据阿伏加德罗定律判断,下列叙述错误的是
| A.x∶y等于甲与乙的相对分子质量之比 |
| B.x∶y等于等质量的甲与乙的分子个数之比 |
| C.x∶y等于同温同压下甲与乙的密度之比 |
| D.y∶x等于同温同体积下等质量的甲与乙的压强之比 |
NA代表阿伏加德罗常数。下列有关NA的叙述中,正确的是( )。
| A.1 mol任何物质所含的分子数均为NA |
| B.14 g氮气所含的氮原子数为NA |
| C.标准状况下,22.4 L水所含的水分子数为NA |
| D.在钠与氯气的反应中,1 mol钠失去电子的数目为2NA |
下图是氨气与氯化氢反应的装置。抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)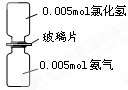
| A.气体反应物的总体积为0.224 L |
| B.产物中所含的N-H键个数为0.015NA |
| C.生成物的物质的量为0.005 mol |
| D.加水溶解后所得溶液中NH4+浓度为0.005 mol.L-1 |
在标准状况下,将某X气体VL溶于水中,得到12mol/L的溶液500mL,则气体的体积V是( )
| A.134.4L | B.67.2L | C.44.8L | D.537.6L |
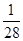 mol N2含有x个N2,则阿伏加德罗常数为( )。
mol N2含有x个N2,则阿伏加德罗常数为( )。
A.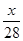 | B.14x mol-1 | C.28x mol-1 | D.28x |