题目内容
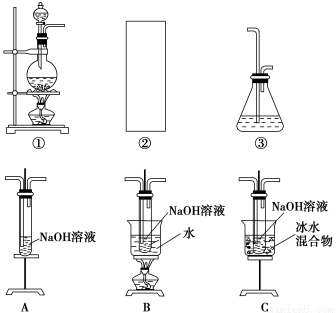
下述实验不能达到预期目的的是 ( )。
编号实验内容实验目的
A将含有HCl杂质的CO2通入饱和Na2CO3溶液中除去CO2中的HCl
B将一定量的KNO3和NaCl的混合液加热并浓缩至有晶体析出,趁热过滤分离出NaCl晶体
C在含有少量FeCl3的MgCl2酸性溶液中加入足量MgO并过滤除去溶液中的FeCl3
D在含有少量Na2S的NaCl溶液中加入AgCl,再过滤除去溶液中的Na2S
A
【解析】选项A,Na2CO3也能吸收CO2,应该用饱和NaHCO3溶液吸收其中的HCl。选项B,由于在较高温度下,KNO3和NaCl溶解度相差较大,可采用浓缩、结晶、过滤的方法分离。选项C,MgO和酸反应促进Fe3+水解形成Fe(OH)3,通过过滤即可除去MgCl2溶液中的FeCl3杂质。选项D,Na2S和AgCl反应生成Ag2S沉淀和NaCl,过滤除去Ag2S和剩余的AgCl,即可除去NaCl溶液中的Na2S。

柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾(FeSO4·7H2O)通过下列反应制备:
FeSO4+Na2CO3=FeCO3↓+Na2SO4
FeCO3+C6H8O7=FeC6H6O7+CO2↑+H2O
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
(1)制备FeCO3时,选用的加料方式是 (填字母),原因是 。
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是 。
(3)将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80 ℃下搅拌反应。①铁粉的作用是 。
②反应结束后,无需过滤,除去过量铁粉的方法是 。
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得柠檬酸亚铁晶体。分离过程中加入无水乙醇的目的是 。
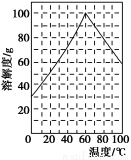
(5)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成柠檬酸亚铁。请结合下图的绿矾溶解度曲线,补充完整由硫铁矿烧渣制备FeSO4·7H2O晶体的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量烧渣中加入足量的稀硫酸充分反应, ,得到FeSO4溶液, ,得到FeSO4·7H2O晶体。