题目内容
按下列要求作答.
(1)①向Ba(OH)2溶液中,逐滴加入NaHSO4溶液使钡离子刚好完全沉淀,请写出反应的离子方程式:______
②向以上溶液中,继续滴加NaHSO4溶液,请写出此步反应的离子方程式:______
(2)用双线桥表示下列反应的电子转移情况.
2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O______.
解:(1)①钡离子刚好完全沉淀,二者以1:1反应,反应生成硫酸钡、NaOH和水,发生的离子反应为H++SO42-+Ba2++OH-═H2O+BaSO4↓,
故答案为:H++SO42-+Ba2++OH-═H2O+BaSO4↓;
②向以上溶液中,继续滴加NaHSO4溶液,发生氢离子与氢氧根离子的反应,该离子反应为H++OH-═H2O,
故答案为:H++OH-═H2O;
(2)Mn元素的化合价由+7价降低为+2价,得到2×5e-,Cl元素的化合价由-1价升高为0,失去10×e-,则双线桥表示反应的电子转移为 ,故答案为:
,故答案为: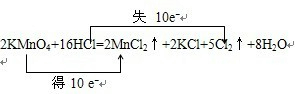 .
.
分析:(1)①钡离子刚好完全沉淀,二者以1:1反应,反应生成硫酸钡、NaOH和水;
②向以上溶液中,继续滴加NaHSO4溶液,发生氢离子与氢氧根离子的反应;
(2)Mn元素的化合价由+7价降低为+2价,得到2×5e-,Cl元素的化合价由-1价升高为0,失去10×e-,以此来解答.
点评:本题考查离子反应及氧化还原反应,明确发生的化学反应是解答本题的关键,注意氧化还原反应中元素的化合价升降,①为易错点,题目难度不大.
故答案为:H++SO42-+Ba2++OH-═H2O+BaSO4↓;
②向以上溶液中,继续滴加NaHSO4溶液,发生氢离子与氢氧根离子的反应,该离子反应为H++OH-═H2O,
故答案为:H++OH-═H2O;
(2)Mn元素的化合价由+7价降低为+2价,得到2×5e-,Cl元素的化合价由-1价升高为0,失去10×e-,则双线桥表示反应的电子转移为
 ,故答案为:
,故答案为: .
.分析:(1)①钡离子刚好完全沉淀,二者以1:1反应,反应生成硫酸钡、NaOH和水;
②向以上溶液中,继续滴加NaHSO4溶液,发生氢离子与氢氧根离子的反应;
(2)Mn元素的化合价由+7价降低为+2价,得到2×5e-,Cl元素的化合价由-1价升高为0,失去10×e-,以此来解答.
点评:本题考查离子反应及氧化还原反应,明确发生的化学反应是解答本题的关键,注意氧化还原反应中元素的化合价升降,①为易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
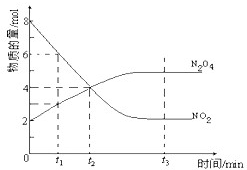 一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8mol NO2,发生如下反应:2NO2(红棕色)?N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答:
一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8mol NO2,发生如下反应:2NO2(红棕色)?N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答: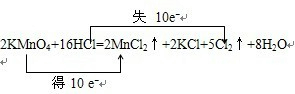
 N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答:
N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答: N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答:
N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答: