题目内容
(14分) 某学生设计了一套验证物质化学性质的实验装置(如图):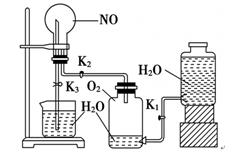
请观察该装置图,完成下列问题:
(1)该实验的目的是
(2)该实验的涉及的化学方程式有
(3)实验用品:实验仪器除铁架台(带铁夹)、储气瓶(两个)、直管活塞(K1、K2)、止水夹(K3)、橡胶管、橡胶塞以及若干玻璃管连件外,还有哪几种(写仪器名称) ____________________。
(4)实验步骤:①按上图连接好仪器装置;②扭开活塞K1和K2,主要现象为 ;
③关闭 ,(填写K1或K2或K3)打开 ,(填写K1或K2或K3), 用手或热毛巾捂住圆底烧瓶,就能使烧瓶产生喷泉。
(1)验证NO与O2反应,NO2与H2O反应 (2分)
(2)2NO+O2=2NO2、3NO2+H2O=2HNO3+NO (6分)
(3)圆底烧瓶和烧杯 (2分)
(4)盛NO的集气瓶内出现红棕色 (2分) K1和K2,K3(2分)
解析试题分析:(1)根据实验装置图可知,NO与O2混合,生成的NO2通入H2O中,所以该实验的目的是:验证NO与O2反应,NO2与H2O反应。
(2)本实验首先发生NO与O2的反应,然后NO2与H2O反应,所以化学方程式为:2NO+O2=2NO2、3NO2+H2O=2HNO3+NO。
(3)根据实验装置图可知,实验仪器除铁架台(带铁夹)、储气瓶(两个)、直管活塞(K1、K2)、止水夹(K3)、橡胶管、橡胶塞以及若干玻璃管连件外,还有:圆底烧瓶和烧杯。
(4)扭开活塞K1和K2后,NO与O2混合,生成NO2,所以反应现象为:盛NO的集气瓶内出现红棕色;关闭K1和K2,打开K3,用手或热毛巾捂住圆底烧瓶,烧瓶内NO2气体体积膨胀,与烧杯内H2O接触发生反应,造成烧瓶内气体压强减小,产生喷泉。
考点:本题考查实验方案的设计与分析、基本仪器和基本操作、化学方程式的书写。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案如图所示装置,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶中,然后打开止水夹,不能出现“喷泉现象”,则物质a、b对应的选项是
| 选项 | a(干燥气体) | b(液体) |
| A | NO | H2O |
| B | Cl2 | 饱和NaCl溶液 |
| C | SO2 | 浓NaOH溶液 |
| D | NH3 | H2O |
为验证铜与稀硝酸反应的还原产物是NO而不是NO2,设计了如下图的装置,以下叙述错误的是
| A.应先打开活塞再从右侧加稀硝酸 |
| B.左侧稀硝酸须注满 |
| C.关闭活塞后铜丝会全部溶解 |
| D.反应停止后打开活塞气体变成红棕色 |
下列有关氯气的叙述中不正确的是( )
| A.氯气是一种黄绿色,有刺激性气味的气体 |
| B.氯气,液氯,氯水是同一种物质 |
| C.氯气能溶于水 |
| D.氯气是一种有毒气体 |
(13分)硫及其化合物有广泛的应用,对SO2性质的研究是高中化学教学的一项重要内容。
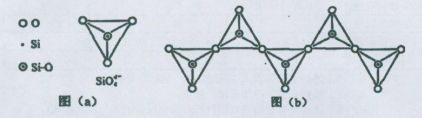
(1)对比研究是一种重要的研究方法。若将硫的单质及部分化合物按如下表所示分成3组,则第2组中物质M的化学式是 。
| 第1组 | 第2组 | 第3组 |
| S(单质) | SO2、H2SO3、M、NaHSO3 | SO3、H2SO4、、Na2SO4、NaHSO4 |
(2)某校化学学习小组用下图所示的实验装置研究SO2的性质。
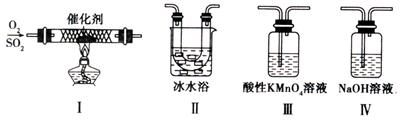
①在装置Ⅰ中发生SO2的催化氧化反应,其化学方程式是 。
②若按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,(已知:SO3熔点 16.8℃; SO2沸点—10℃。)装置Ⅱ的作用是 ;装置Ⅲ中溶液逐渐褪色,生成Mn2+的同时pH降低,则该反应的离子方程式是 。
③若按Ⅰ、Ⅱ、Ⅳ的顺序连接装置,如果装置Ⅳ中有30mL 2.5mol/LNaOH溶液,反应后增重4.8g,则装置Ⅳ中发生反应的化学方程式是 。
在化学课上围绕浓硫酸的化学性质进行了如下实验探究,将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质。
请回答下列问题:
(1)生成的黑色物质(单质)是 (填化学式)。
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,这种刺激性气味的气体成分是 (填化学式),反应的化学方程式为 。
(3)据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有 (填序号)。
| A.酸性 | B.吸水性 | C.脱水性 | D.强氧化性 |
(5)能否用澄清石灰水鉴别这两种气体? (填“能”或“不能”),若不能,请填写两种能鉴别的试剂 。