题目内容
【题目】丙烯和乙烯一样,都是重要的化工原料。由丙烯经下列反应可得到F、G两种高分子化合物,它们都是常用的塑料。

(1)丙烯生成A和F的反应方程式分别为______、______。
(2)D生成E的反应是原子利用率100%的反应,且D不能使溴的四氯化碳溶液褪色,则D的结构简式为________。
(3)一定条件下,两分子E之间脱去一分子水生成一种具有芳香气味的物质。请写出反应的化学方程式_________。
(4)下列说法不正确的是_________。
A.丙烯没有同分异构体
B.聚丙烯能使高锰酸钾酸性溶液褪色
C.1 mol E与足量金属钠反应可以生成22.4 L氢气(标准状况)
D.化合物G属于酯类
【答案】CH3CH![]() CH2+Br2
CH2+Br2![]()
![]() nCH3CH
nCH3CH![]() CH2
CH2![]()
![]()
![]()
![]()
![]()
![]() +H2O AB
+H2O AB
【解析】
丙烯中含有碳碳双键,能发生加聚反应,即F的结构简式为![]() ,D与氢气发生加成反应,得到E,根据E的结构简式,以及问题(2),推出D的结构简式为
,D与氢气发生加成反应,得到E,根据E的结构简式,以及问题(2),推出D的结构简式为![]() ,丙烯与Br2发生加成反应,得到A,即A的结构简式为CH3CHBrCH2Br,A在NaOH水溶液中发生水解反应,得到B为CH3CH(OH)CH2OH,然后连续被氧化,得到D;
,丙烯与Br2发生加成反应,得到A,即A的结构简式为CH3CHBrCH2Br,A在NaOH水溶液中发生水解反应,得到B为CH3CH(OH)CH2OH,然后连续被氧化,得到D;
丙烯中含有碳碳双键,能发生加聚反应,即F的结构简式为![]() ,D与氢气发生加成反应,得到E,根据E的结构简式,以及问题(2),推出D的结构简式为
,D与氢气发生加成反应,得到E,根据E的结构简式,以及问题(2),推出D的结构简式为![]() ,丙烯与Br2发生加成反应,得到A,即A的结构简式为CH3CHBrCH2Br,A在NaOH水溶液中发生水解反应,得到B为CH3CH(OH)CH2OH,然后连续被氧化,得到D;
,丙烯与Br2发生加成反应,得到A,即A的结构简式为CH3CHBrCH2Br,A在NaOH水溶液中发生水解反应,得到B为CH3CH(OH)CH2OH,然后连续被氧化,得到D;
(1)丙烯发生加聚反应,其反应方程式为nCH3CH![]() CH2
CH2![]()
![]() ,丙烯中含有碳碳双键,能与Br2发生加成反应,其反应方程式为 CH3CH
,丙烯中含有碳碳双键,能与Br2发生加成反应,其反应方程式为 CH3CH![]() CH2+Br2
CH2+Br2![]()
![]() ;
;
(2)由上述分析,推出B的结构简式为![]()
![]() ,D不能使溴的四氯化碳溶液褪色,说明不含碳碳双键,D为
,D不能使溴的四氯化碳溶液褪色,说明不含碳碳双键,D为![]() ,D生成E原子利用率为100%,发生加成反应,D经加氢还原生成E;
,D生成E原子利用率为100%,发生加成反应,D经加氢还原生成E;
(3)两分子的E之间脱去1分子水生成具有芳香气味的物质,该物质为酯,即发生酯化反应,反应方程式为![]()
![]()
![]() +H2O
+H2O
(4)A、单烯烃与环烷烃互为同分异构体,丙烯与环丙烷是同分异构体,故A说法错误;
B、丙烯加聚后不再含有碳碳双键,不能使酸性高锰酸钾溶液褪色,故B说法错误;
C、E中含有官能团是-OH和-COOH,能与Na发生产生H2的官能团是羟基和羧基,即1molE与足量金属钠发生反应,产生H2的物质的量为1mol,即标准状况下1molH2的体积为22.4L,故C说法正确;
D、E生成G发生缩聚反应,实质为酯化反应,因此G为酯,故D说法正确。

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案【题目】硼酸三甲酯用作柠檬类水果的熏蒸剂。实验室合成硼酸三甲酯的原理及装置如下:
硼酸三甲酯 | 甲醇 | |
溶解性 | 与乙醚、甲醇混溶,能水解 | 与水混溶 |
沸点/℃ | 68 | 64 |
硼酸三甲酯与甲醇混合物的共沸点为54℃ | ||
Na2B4O7·10H2O+2H2SO4+16CH3OH![]() 2NaHSO4+4[(CH3O)3B+CH3OH]+17H2O
2NaHSO4+4[(CH3O)3B+CH3OH]+17H2O
实验步骤如下:
①在圆底烧瓶中加入44.8g甲醇和19.1gNa2B4O7·10H2O (硼砂,式量为382),然后缓慢加入浓H2SO4并振荡;加热烧瓶中的液体;通过分馏柱回流一段时间。
②先接收51~55℃的馏分,再接收55~60℃的馏分。
③将两次馏分合并,加入氯化钙进行盐析分层,上层为硼酸三甲酯,分离。
④精馏得高纯硼酸三甲酯19.2g。
回答下列问题:
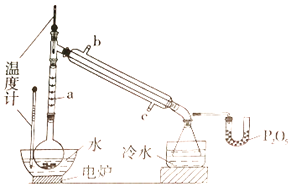
(1)图中仪器a的名称为____________;直形冷凝管冷却水应从____________(填“b”或“c”)接口进入。
(2)本实验加热方式为____________,优点是____________。
(3)加入氯化钙盐析分层的主要目的是____________。
(4)U型管中P2O5的作用是_____________________________________。
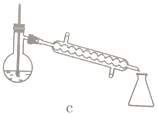
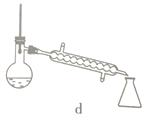
(5)步骤④的仪器选择及安装都正确的是____________ (填标号),应收集____________℃的馏分。


(6)本次实验的产率是____________。
【题目】有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验装置 |
|
|
|
|
部分实验现象 | a极质量减小b极质量增加 | 溶液中的 | d极溶解c极有气体产生 | 电子从d极流向a极 |
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c
【题目】下列实验操作、现象和所得结论错误的是 ( )
选项 | 操作 | 现象 | 结论 |
A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状炭,并放出有刺激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
B | 向久置的Na2SO3溶液中加入足量Ba(NO3)2溶液,再加入足量稀盐酸 | 先出现白色沉淀,然后部分沉淀溶解 | 部分Na2SO3被氧化 |
C | 某溶液中滴加K3[Fe(CN)6]溶液 | 产生蓝色沉淀 | 原溶液中有Fe2+,可能有Fe3+ |
D | 向等浓度的KCl、KI混合液中逐滴滴加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
A. AB. BC. CD. D