题目内容
【题目】下列关系不正确的是( )
A.等质量的烃完全燃烧消耗氧量:甲烷>乙烷>乙烯>苯
B.熔点:正戊烷>2,2–二甲基戊烷>2,3–二甲基丁烷>丙烷
C.密度:CCl4>CH2Cl2>H2O>苯
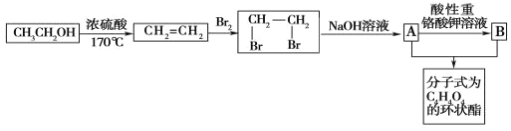
D.![]() 的一氯取代产物有4种
的一氯取代产物有4种
【答案】B
【解析】
A. 等质量的烃完全燃烧,若烃中含有的H元素的质量分数最大,消耗的氧气最多,选项中H的质量分数大小顺序为甲烷>乙烷>乙烯>苯,则耗氧量大小顺序为甲烷>乙烷>乙烯>苯,故A正确;
B. 有机物中碳原子数越多,相对分子质量越大,则熔点越高,选项中碳原子个数多少顺序为:2,2–二甲基戊烷>2,3–二甲基丁烷>正戊烷>丙烷,则熔点大小顺序为2,2–二甲基戊烷>2,3–二甲基丁烷>正戊烷>丙烷,故B错误;
C. 有机物中相对分子质量越大,密度越小,则选项中密度大小关系为:CCl4>CH2Cl2>H2O>苯,故C正确;
D. ![]() 是对称的结构,一氯取代产物有4种,故D正确;
是对称的结构,一氯取代产物有4种,故D正确;
题目要求选择错误的,故选B。

【题目】温下,将四种不同的一元酸(用 HA 代表)分别和 NaOH 溶液等体积混合。 两种溶液的物质的量浓度和混合溶液的 pH 如下表所示:
实验 | HA 物质的量 | NaOH 物质的量 | 混合后溶 |
编号 | 浓度/(mol·L-1) | 浓度/(mol·L-1) | 液的 pH |
甲 | 0.1 | 0.1 | pH=a |
乙 | 0.12 | 0.1 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=11 |
(1)从甲组情况分析,如何判断 HA 是强酸还是弱酸?___________
(2)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是:____________________
(3)分析丁组实验数据,写出混合溶液中下列算式的精确结果(列式表示):c(Na+)-c(A-)=______mol·L-1。
(4)某二元酸(化学式用 H2B 表示)在水中的电离方程式是:H2B=H++HB- HB-![]() H++B2-
H++B2-
在0.1 mol·L-1 的 Na2B 溶液中,下列粒子浓度关系式正确的是________。
A.c(B2-)+c(HB-)=0.1 mol·L-1 B.c(B2-)+c(HB-)+c(H2B)=0.1 mol·L-1
C.c(OH-)=c(H+)+c(HB-) D.c(Na+)+c(H+)=c(OH-)+c(HB-)