题目内容
【题目】某科研小组利用甲醇燃料电池进行如下电解实验,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法不正确的是

A. 甲池中通入CH3OH的电极反应:CH3OH-6e-+8OH-=CO32-+6H2O
B. 甲池中消耗560mLO2(标准状况下),理上乙池Ag电极增重3.2g
C. 反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度
D. 丙池右侧Pt电极的电极反应式:Mg2++2H2O+2e-=Mg(OH)2↓+H2↑
【答案】C
【解析】A.在燃料电池中,负极上CH3OH发生失电子的氧化反应,碱性条件下生成CO32-和H2O;B. 乙装置中,在阴极上是Cu离子放电,减小的Cu离子是0.05mol,所以理上乙池Ag电极增重的质量应该是0.05molCu的质量;C.电解池中,电解后的溶液复原遵循:出什么加什么的思想;D. 丙池右侧Pt电极为阴极,氢离子得电子变为氢气.
A. 在燃料电池中,负极是甲醇发生失电子的氧化反应,在碱性电解质下的电极反应为CH3OH-6e-+8OH-=CO32-+6H2O,故A正确;B.甲池中根据电极反应:O2+2H2O+4e=4OH,所以消耗560mL(标准状况下0.025mol)O2,则转移电子0.1mol,根据乙装置中,在阴极上是Cu离子放电,减小的Cu离子是0.05mol,所以理上乙池Ag电极增重的质量应该是0.05×64g/mol=3.2g固体,故B正确;C. 电解池乙池中,电解硫酸铜和水,生成硫酸、铜和氧气,要想复原,要加入氧化铜或碳酸铜,故C错误;D. 丙池右侧Pt电极为阴极,氢离子得电子变为氢气,电极反应式为:Mg2++2H2O+2e-=Mg(OH)2↓++H2↑,故D正确;答案选C.

 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案【题目】下列实验现象不能说明相应的化学反应一定是放热反应的是
选项 | A | B | C | D |
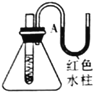
反应装置 |
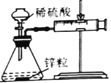
|
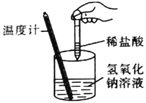
|
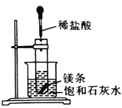
|
|
实验现象 | 试管中生石灰和水混合后,A处红色水柱下降 | 反应开始后,针筒活塞向右移动 | 温度计的水银柱不断上升 | 饱和石灰水变浑浊 |
A. A B. B C. C D. D