题目内容
测血钙的含量时,可将2.0 mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀。将沉淀用稀硫酸处理得H2C2O4后,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+,若终点时用去20.0 mL 1.0×10-4 mol·L-1的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式 。
(2)判断滴定终点的方法是 。
(3)计算:血液中含钙离子的浓度为 g·mL-1。
(1)写出用KMnO4滴定H2C2O4的离子方程式 。
(2)判断滴定终点的方法是 。
(3)计算:血液中含钙离子的浓度为 g·mL-1。
(1)2Mn+5H2C2O4+6H+ 2Mn2++10CO2↑+8H2O
2Mn2++10CO2↑+8H2O
(2)当滴入1滴酸性KMnO4溶液后溶液由无色变为浅紫色,且半分钟内不褪色
(3)1.0×10-4
 2Mn2++10CO2↑+8H2O
2Mn2++10CO2↑+8H2O(2)当滴入1滴酸性KMnO4溶液后溶液由无色变为浅紫色,且半分钟内不褪色
(3)1.0×10-4
因为滴加酸性KMnO4溶液至反应完毕过量时,会使溶液呈紫色,故可用滴入一滴酸性KMnO4溶液由无色变为浅紫色且半分钟不褪色的方法来判断终点。由题意知可能发生反应的离子方程式为:2Mn+5H2C2O4+6H+ 2Mn2++10CO2↑+8H2O、Ca2++C2
2Mn2++10CO2↑+8H2O、Ca2++C2 CaC2O4↓、CaC2O4+2H+
CaC2O4↓、CaC2O4+2H+ Ca2++H2C2O4。
Ca2++H2C2O4。
设2 mL血液中含Ca2+的物质的量为x,则
5Ca2+~5CaC2O4~5H2C2O4~2Mn
5 2
x 20.0×10-3 L×1.0×10-4 mol·L-1
x=5.0×10-6 mol,1 mL血液中Ca2+的浓度为=1.0×10-4 g·mL-1。
 2Mn2++10CO2↑+8H2O、Ca2++C2
2Mn2++10CO2↑+8H2O、Ca2++C2 CaC2O4↓、CaC2O4+2H+
CaC2O4↓、CaC2O4+2H+ Ca2++H2C2O4。
Ca2++H2C2O4。设2 mL血液中含Ca2+的物质的量为x,则
5Ca2+~5CaC2O4~5H2C2O4~2Mn
5 2
x 20.0×10-3 L×1.0×10-4 mol·L-1
x=5.0×10-6 mol,1 mL血液中Ca2+的浓度为=1.0×10-4 g·mL-1。

练习册系列答案
相关题目
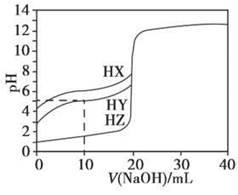
 +c(Z-)+c(OH-)
+c(Z-)+c(OH-)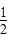 CH4(g)+O2(g)=
CH4(g)+O2(g)=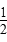 CO2(g)+H2O(l)ΔH=-890 kJ/mol
CO2(g)+H2O(l)ΔH=-890 kJ/mol H2(g)+
H2(g)+