题目内容
实验室用浓盐酸和二氧化锰制备氯气并用所制氯气制备少量氯水的装置图如下,回答有关问题.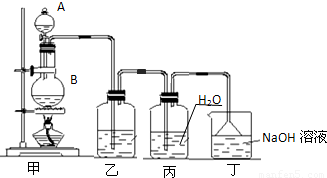
(1)从仪器A向仪器B中加入浓盐酸的操作方法是______.反应中控制氯气产生速率大小的方法是______.
(2)装置乙中盛放的试剂是______,其作用是______.
(3)写出氯气与水反应的化学方程式______.
(4)某同学设计了一个实验方案以证明新制氯水中含有次氯酸.他所用的试剂如下:
新制氯水 0.5mol.L-1CaCl2溶液 品红溶液 CaCO3粉末
请你协助完成实验方案.
步骤一:取5mL0.5mol.L-1CaCl2溶液于试管中,滴入3滴品红溶液,振荡,溶液不褪色.
步骤二:取5mL新制氯水于试管中,______.
步骤三:______.
说明新制氯水中存在次氯酸的实验现象是______.
(5)设计步骤一的理由是______.
【答案】分析:(1)根据分液漏斗的使用方法和活塞的作用来回答;
(2)除去氯气中的氯化氢杂质可以用饱和食盐水;
(3)氯气和水反应生成盐酸和次氯酸;
(4)根据氯水的成分以及各个成分的性质来回答;
(5)根据实验结论得出的干扰项:氯化钙的存在是否干扰实验结果来分析.
解答:解:(1)根据分液漏斗的使用方法:取下分液漏斗上口玻璃塞,旋动活塞,即可放下液体,为了控制液体的流速,可以通过控制分液漏斗的旋塞来控制浓盐酸的加入速度来控制氯气的产生速率,故答案为:取下分液漏斗上口玻璃塞,旋动活塞,即可放下液体;通过控制浓盐酸的加入速度来控制氯气的产生速率;
(2)除去氯气中的氯化氢杂质可以用饱和食盐水,故答案为:饱和食盐水; 除去氯气中的氯化氢;
(3)氯气和水反应生成盐酸和次氯酸,即Cl2+H2O=HCl+HClO,故答案为:Cl2+H2O=HCl+HClO;
(4)氯水中含有盐酸和次氯酸,其中的盐酸可以和碳酸钙反应生成氯化钙、水以及二氧化碳,根据对比试验,氯化钙不能使品红退色来证明使品红退色的是次氯酸,
故答案为:加入碳酸钙粉末充分反应至溶液无色;取上层清液于另一试管中加入3滴品红溶液,振荡;品红溶液褪色;
(5)设计步骤一:取5mL0.5mol.L-1CaCl2溶液于试管中,滴入3滴品红溶液,振荡,溶液不褪色,说明氯化钙不会使品红退色,这样氯水与碳酸钙反应后生成氯化钙溶液,为的是证明品红溶液褪色是次氯酸的作用,故答案为:氯水与碳酸钙反应后生成氯化钙溶液,为证明品红溶液褪色是次氯酸的作用,须实验证明氯化钙溶液不具漂白性(或“排除氯化钙溶液的干扰”).
点评:本题考查是教材中的基本实验中的知识,非常重要,难度大,要求学生学习时必须全面掌握基础知识.
(2)除去氯气中的氯化氢杂质可以用饱和食盐水;
(3)氯气和水反应生成盐酸和次氯酸;
(4)根据氯水的成分以及各个成分的性质来回答;
(5)根据实验结论得出的干扰项:氯化钙的存在是否干扰实验结果来分析.
解答:解:(1)根据分液漏斗的使用方法:取下分液漏斗上口玻璃塞,旋动活塞,即可放下液体,为了控制液体的流速,可以通过控制分液漏斗的旋塞来控制浓盐酸的加入速度来控制氯气的产生速率,故答案为:取下分液漏斗上口玻璃塞,旋动活塞,即可放下液体;通过控制浓盐酸的加入速度来控制氯气的产生速率;
(2)除去氯气中的氯化氢杂质可以用饱和食盐水,故答案为:饱和食盐水; 除去氯气中的氯化氢;
(3)氯气和水反应生成盐酸和次氯酸,即Cl2+H2O=HCl+HClO,故答案为:Cl2+H2O=HCl+HClO;
(4)氯水中含有盐酸和次氯酸,其中的盐酸可以和碳酸钙反应生成氯化钙、水以及二氧化碳,根据对比试验,氯化钙不能使品红退色来证明使品红退色的是次氯酸,
故答案为:加入碳酸钙粉末充分反应至溶液无色;取上层清液于另一试管中加入3滴品红溶液,振荡;品红溶液褪色;
(5)设计步骤一:取5mL0.5mol.L-1CaCl2溶液于试管中,滴入3滴品红溶液,振荡,溶液不褪色,说明氯化钙不会使品红退色,这样氯水与碳酸钙反应后生成氯化钙溶液,为的是证明品红溶液褪色是次氯酸的作用,故答案为:氯水与碳酸钙反应后生成氯化钙溶液,为证明品红溶液褪色是次氯酸的作用,须实验证明氯化钙溶液不具漂白性(或“排除氯化钙溶液的干扰”).
点评:本题考查是教材中的基本实验中的知识,非常重要,难度大,要求学生学习时必须全面掌握基础知识.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
下图所示装置常用于实验室制取某些气体。现实验室有下列药品:
①二氧化锰;②碱石灰;③大理石;④氯化钠;⑤双氧水;⑥浓氨水;⑦浓盐酸;⑧蒸馏水。
请根据如图所示的实验装置结合实验原理回答下列问题。

(1)请在下表中填入利用该装置可以制取的气体和所需药品的编号(表格可以不填全)。
可以制取的气体(填化学式) | 所需药品的编号 |
|
|
|
|
|
|
|
|
(2)请简述检查该装置气密性的正确实验操作。
(3)资料显示:“氨气可在纯氧中安静燃烧……”某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去),进行氨气与氧气在不同条件下反应的实验。

①将产生的氨气与过量的氧气通到装置A(催化剂为铂石棉)中,用酒精喷灯加热。请写出氨催化氧化的化学方程式是______________________________________;
②将过量的氧气与氨气分别从B装置中a、b两管进气口通入到装置B中,并在b管上端点燃氨气。则两气体通入的先后顺序是___________________________________________,理由是________________________________________________________。
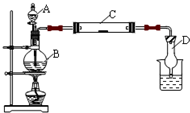 (2011?松江区模拟)为了制得氯气并探究氯气的一些化学性质,某学生用如图所示装置进行有关实验,打开A的玻璃塞,将A中浓盐酸溶液逐滴加入装有二氧化锰的B中.试回答:
(2011?松江区模拟)为了制得氯气并探究氯气的一些化学性质,某学生用如图所示装置进行有关实验,打开A的玻璃塞,将A中浓盐酸溶液逐滴加入装有二氧化锰的B中.试回答: 在酸性条件下有很强的氧化性,它在常温下就能将
在酸性条件下有很强的氧化性,它在常温下就能将 氧化为
氧化为 ,
, 被还原成
被还原成 ,写出高锰酸钾跟浓盐酸在室温下反应制取氯气的化学方程式______________________________.
,写出高锰酸钾跟浓盐酸在室温下反应制取氯气的化学方程式______________________________.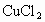 作催化剂,在450℃利用空气中的氧气跟氯化氢反应制氯气.反应的化学方程式是_______
作催化剂,在450℃利用空气中的氧气跟氯化氢反应制氯气.反应的化学方程式是_______