题目内容
【题目】甲胺铅碘(CH3NH3PbI3)用作全固态钙钛矿敏化太阳能电池的敏化剂,可由CH3NH2、PbI2及HI为原料合成,回答下列问题:
(1)制取甲胺的反应为CH3OH(g)+NH3(g)![]() CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
共价键 | C—O | H—O | N—H | C—N | C—H |
键能/kJ·mol-1 | 351 | 463 | 393 | 293 | 414 |
则该反应的ΔH=____kJ·mol-1。
(2)上述反应中所需的甲醇工业上利用水煤气合成CO(g)+2H2(g)![]() CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
CH3OH(g) ΔH<0。在一定条件下,将1 mol CO和2 mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
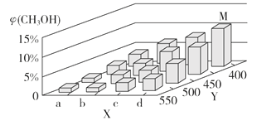
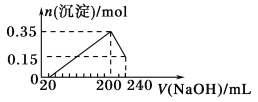
①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为___。
②X轴上a点的数值比b点____ (填“大”或“小”)。某同学认为上图中Y轴表示温度,你认为他判断的理由是_________________。
(3)工业上可采用CH3OH CO+2H2 来制取高纯度的CO和H2。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。
CO+2H2 来制取高纯度的CO和H2。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。
甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式 A:CH3OH* →CH3O* +H* Ea= +103.1kJ·mol-1
方式 B:CH3OH* →CH3* +OH* Eb= +249.3kJ·mol-1
由活化能E值推测,甲醇裂解过程主要历经的方式应为___(填A、B)。
下图为计算机模拟的各步反应的能量变化示意图。
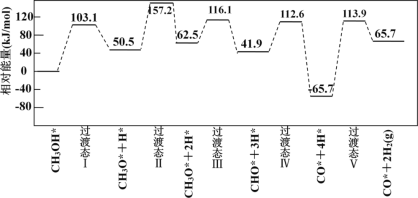
该历程中,放热最多的步骤的化学方程式为________。
(4)PbI2与金属锂以LiI-Al2O3固体为电解质组成锂碘电池,其结构示意图如下,电池总反应可表示为:2Li+PbI2=2LiI+Pb,则b极上的电极反应式为:_____。

(5)CH3NH2的电离方程式为CH3NH2+H2O![]() CH3NH3++OH-电离常数为kb,已知常温下pkb=-lgkb=3.4,则常温下向CH3NH2溶液滴加稀硫酸至c(CH3NH2)=c(CH3NH3+)时,溶液pH=______。
CH3NH3++OH-电离常数为kb,已知常温下pkb=-lgkb=3.4,则常温下向CH3NH2溶液滴加稀硫酸至c(CH3NH2)=c(CH3NH3+)时,溶液pH=______。
【答案】-12 25% 小 随着Y值的增大,φ(CH3OH)减小,平衡CO(g)+2H2(g) ![]() CH3OH(g)向逆反应方向进行,故Y为温度 A CHO*+3H*=CO*+4H*(或CHO*=CO*+H*) PbI2+2e-=Pb+2I- 或PbI2+2e-+2Li+=Pb+2LiI 10.6
CH3OH(g)向逆反应方向进行,故Y为温度 A CHO*+3H*=CO*+4H*(或CHO*=CO*+H*) PbI2+2e-=Pb+2I- 或PbI2+2e-+2Li+=Pb+2LiI 10.6
【解析】
(1)反应热等于反应物总键能减去生成物总键能,则CH3OH(g)+NH3(g)CH3NH2(g)+H2O(g)的△H=[351+414×3+463+393×3-(414×3+293+393×2-463×2)]kJ/mol=-12kJ/mol;
(2)①初始投料为1 mol CO和2 mol H2,设转化的CO的物质的量为x,列三段式有:
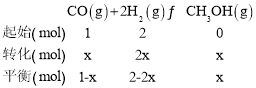
CH3OH的体积分数为10%,则有![]() =10%,解得x=0.25mol,所以CO的转化率为
=10%,解得x=0.25mol,所以CO的转化率为![]() =25%;
=25%;
②X表示压强,该反应是气体体积减小的反应,增大压强,平衡向正反应方向移动,则CH3OH的体积分数φ(CH3OH)也越大,b点CH3OH的体积分数φ(CH3OH)大于a点CH3OH的体积分数φ(CH3OH),则X轴上a点的数值比b点小;由图可知,随着Y值减小,CH3OH的体积分数φ(CH3OH)增大,该反应是放热反应,降低温度,平衡向正反应方向移动,CH3OH的体积分数φ(CH3OH)也越大,故Y表示温度;
(3)方式A所需活化能更低,反应速率更快,更容易进行,所以甲醇裂解过程主要历经的方式应为A;由图象可知,相对能量从112降至-65时,放出的热量最多,放热最多的步骤的化学方程式为CHO*+3H*=CO*+4H*(或CHO*=CO*+H*);
(4)根据电池总反应可知Li被氧化,应为负极,则b即正极,得电子发生还原反应,根据总反应可知电极反应为PbI2+2e-=Pb+2I- 或PbI2+2e-+2Li+=Pb+2LiI;
(5)根据题意kb=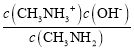 =10-3.4,所以当c(CH3NH2)=c(CH3NH3+)时,溶液中c(OH-)=10-3.4mol/L,则c(H+)=10-10.6mol/L,所以pH=10.6。
=10-3.4,所以当c(CH3NH2)=c(CH3NH3+)时,溶液中c(OH-)=10-3.4mol/L,则c(H+)=10-10.6mol/L,所以pH=10.6。

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案【题目】已知25 ℃时部分弱电解质的电离平衡常数数据如下表:
弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
电离平衡常数 | 1.3×101 | 1.7×105 | 6.2×1010 | K1=4.3×107 K2=5.6×1011 |
回答下列问题:
(1)写出碳酸的第一级电离平衡常数表达式:K1=_______________________。
(2)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为________(填字母)。
(3)常温下,0.1 mol·L1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是________(填序号)
A.[H+] B.[H+]/[CH3COOH]
C.[H+]·[OH] D.[OH]/[H+]
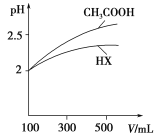
(4)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
(5)写出少量CO2通入次氯酸钠溶液中的离子方程式:_____________________________。
【题目】某研究性学习小组的同学在学习了二氧化碳与过氧化钠的反应后,对过氧化钠与二氧化硫的反应进行实验探究。
(1)提出假设:
假设1. 固体产物是Na2SO3
假设2. _________________________
假设3. 固体产物是Na2SO3和Na2SO4的混合物。
(2)实验验证:用如图所示装置对上述假设进行实验。
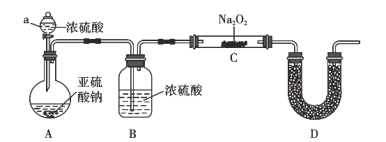
(1)仪器a的名称为__________,装置A中发生反应的化学方程式为:________________________。
(2)装置B的作用为________________________,装置D中试剂的名称为________。
(3)装置C中固体完全反应后,得到白色固体,进行如下实验。
实验操作 | 预期现象与结论 |
步骤1.取少量白色固体于试管中,加入足量的稀盐酸,将生成的气体通入品红溶液。 | 若_____________,说明白色固体中含有Na2SO3。 |
步骤2.在步骤1反应后的溶液中加入________ | 若_____________,说明白色固体中含有Na2SO4。 |
通过实验探究发现上述两个实验现象均有,则说明假设3正确。