题目内容
【题目】元素周期表中短周期的一部分如图,关于X、Y、Z、W、Q说法正确的是
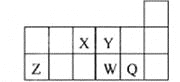
A. 元素Y与元素Z的最高正化合价之和的数值等于9
B. 原子半径的大小顺序为:W>Z>Y
C. 离子半径的大小顺序为:W2->Y2->Z3+
D. W的气态氢化物的热稳定性和还原性均比Q的氢化物的强
【答案】C
【解析】试题分析:根据元素在周期表中的相对位置可知X、Y、Z、W、Q分别是N、O、Al、S、Cl。A、氧元素无正价,A不正确;B、同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则原子半径的大小顺序为:Al>S>O,B不正确;C、离子核外电子层数越多离子半径越大,核外电子排布相同的离子,离子半径随原子序数的增大而减小,则离子半径的大小顺序为:S2->O2->Al3+,C正确;D、非金属性越弱氢化物的稳定性越弱,则热稳定性:H2S﹤HCl,但还原性:H2S﹥HCl,D不正确,答案选C。

 名校课堂系列答案
名校课堂系列答案【题目】能源与材料、信息被称为现代社会发展的三大支柱,化学与能源有着密切联系。
(1)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1):
化学键 | H—H | Cl-Cl | H—Cl |
键能 | 436 | 243 | 431 |
请根据以上信息写出氢气在氯气中燃烧生成氯化氢气体的热化学方程式_______。
(2)天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷。
①以甲烷、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池的负极反应式为___________________________。
②将质量相等的铁棒和石墨棒分别插入CuCl2溶液中,铁棒接甲烷燃料电池负极,石墨棒接该电池正极,一段时间后测得铁棒比石墨棒增加了6.4克。写出铁棒电极上发生的电极反应式________; 则理论上消耗CH4的体积在标准状况下为_____。
(3)如图所示的实验装置中,丙为用碘化钾溶液润湿的滤纸,m、n为夹在滤纸两端的铂夹;丁为直流电源,x、y为电源的两极;G为电流计;A、B、C、D四个电极均为石墨电极。若在两试管中充满H2SO4溶液后倒立于H2SO4溶液的水槽中,闭合K2,断开K1。

①丙电解时反应的离子方程式为______________。
②继续电解一段时间后,甲池中A、B极均部分被气体包围,此时断开K2,闭合K1,电流计G指针发生偏转,则B极的电极反应式为__________________,C极的电极反应为__________________。