题目内容
5.下列说法正确的是( )| A. | 化学反应的速率越大,化学反应的限度越大 | |
| B. | 质量数不同的原子互称同位素 | |
| C. | 糖类、油脂、蛋白质都能发生水解 | |
| D. | 油脂有油和脂肪之分,但都属于酯 |
分析 A.化学反应速率表示的化学反应进行的快慢程度,化学反应速率与化学限度没有必然关系;
B.有相同质子数,不同中子数或同一元素的不同核素互为同位素;
C.糖类中的单糖不能发生水解反应;
D.油脂是高级脂肪酸甘油酯.
解答 解:A.化学反应速率与化学反应限度之间不存在必然关系,不能根据反应速率大小判断反应限度,故A错误;
B.有相同质子数,不同中子数或同一元素的不同核素互为同位素,故B错误;
C.糖类中的单糖,比如葡萄糖和固体═果糖不能发生水解反应,故C错误;
D.油脂是高级脂肪酸甘油酯,液体的叫做油,固体的是脂肪,故D正确,故选D.
点评 本题主要考查的是化学反应速率的意义、同位素的概念、糖类的性质以及油脂的组成,难度不大.

练习册系列答案
相关题目
10.下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 室温下,向NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) | |
| B. | 0.1mol•L-1NaHCO3溶液:c(Na+)>c(OH-)>c(HCO3-)>c(H+) | |
| C. | NaHSO3溶液:c(OH-)+c(SO32-)=c(HSO3-)+2c(H2SO3)+c(H+) | |
| D. | 25℃时,浓度均为0.1mol•L-1的CH3COOH、CH3COONa混合溶液,pH=4.75:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |
11.下列实验操作中,不是主要从安全因素考虑的是( )
| A. | 给试管里的固体加热时,试管口应略向下倾斜,外壁干燥后再预热 | |
| B. | 给试管里的液体加热时.试管口应略向上倾斜(约45°),外壁干燥后再预热 | |
| C. | 加热后的蒸发皿,要用坩埚钳夹持 | |
| D. | 盛装浓硫酸的铁桶,用水冲洗,并用打火机照明 |
20.某学生做同主族元素性质递变规律的实验时,自己设计了一套实验方案,并记录了有关实验现象.现在请你帮助该学生整理并完成实验报告.
(1)实验目的:探究同一主族元素性质的递变规律
(2)实验用品:药品:氯水、溴水、溴化钠溶液、碘化钾溶液、四氯化碳.
仪器:①试管;②胶头滴管(请填写两件主要的玻璃仪器)
(3)实验内容:
(4)实验结论:同一主族元素,自上而下,元素的非金属性依次减弱.
(5)问题和讨论:请用结构理论简单说明得出上述结论的原因.同一主族元素,自上而下,元素原子的电子层数增多,原子半径增大,原子核对最外层电子的吸引力逐渐减弱.
(1)实验目的:探究同一主族元素性质的递变规律
(2)实验用品:药品:氯水、溴水、溴化钠溶液、碘化钾溶液、四氯化碳.
仪器:①试管;②胶头滴管(请填写两件主要的玻璃仪器)
(3)实验内容:
| 序号 | 实验方案 | 实验现象 |
| ① | 将少量氯水滴入盛有少量NaBr溶液的试管中,振荡;再滴入少量四氯化碳,振荡 | 加入氯水后,溶液由无色变为橙色,滴入四氯化碳后,水层颜色变浅,四氯化碳层(下层)变为橙红色 |
| ② | 将少量溴水滴入盛有少量KI溶液的试管中,振荡;再滴入少量四氯化碳,振荡 | 加入溴水后,溶液由无色变为黄色,滴入四氯化碳后,水层颜色变浅,四氯化碳层(下层)变为紫色 |
(5)问题和讨论:请用结构理论简单说明得出上述结论的原因.同一主族元素,自上而下,元素原子的电子层数增多,原子半径增大,原子核对最外层电子的吸引力逐渐减弱.
10. 某同学做“证明鸡蛋壳的主要成分是碳酸盐”的实验时,设计了如图所示的方案.经检验装置气密性合格并加入试剂.下列说法中不正确的是( )
某同学做“证明鸡蛋壳的主要成分是碳酸盐”的实验时,设计了如图所示的方案.经检验装置气密性合格并加入试剂.下列说法中不正确的是( )
 某同学做“证明鸡蛋壳的主要成分是碳酸盐”的实验时,设计了如图所示的方案.经检验装置气密性合格并加入试剂.下列说法中不正确的是( )
某同学做“证明鸡蛋壳的主要成分是碳酸盐”的实验时,设计了如图所示的方案.经检验装置气密性合格并加入试剂.下列说法中不正确的是( )| A. | Ⅰ中发生的现象为鸡蛋壳逐渐溶解,产生大量气泡 | |
| B. | Ⅱ中的澄清石灰水变浑浊 | |
| C. | Ⅲ中紫色石蕊试液变红 | |
| D. | 鸡蛋壳发生了分解反应 |
14.某课外小组对一些金属单质和化合物的性质进行研究.
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分:
按反应类型写出实验中发生反应的化学方程式各一个(是离子反应的只写离子方程式)
置换反应2Al+3Cu2+=2Al3++3Cu;化合反应2Cu+O2+CO2+H2O=Cu2(OH)2CO3.
(2)工业上可用铝与软锰矿(主要成分为MnO2)反应来冶炼金属锰.MnO2在H2O2分解反应中作催化剂.若将适量MnO2加入酸化后的H2O2溶液中,MnO2溶解产生Mn2+.该反应的离子方程式是MnO2+H2O2+2H+═Mn2++O2↑+2H2O.
(3)某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾.其设计的实验过程如图所示:

①铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于c上(用以下所给仪器的编号填入,下同),取用坩埚应使用e,灼烧后的坩埚应放在b上,不能直接放在桌面上.实验所用仪器:a.蒸发皿 b.石棉网 c.泥三角 d.表面皿 e.坩埚钳 f.试管夹
②由粗制氧化铜通过两种途径制取胆矾,通过途径Ⅱ实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、加热蒸发、冷却结晶、过滤洗涤、自然干燥,与途径Ⅰ相比,途径Ⅱ有明显的两个优点是:产生等量胆矾途径Ⅱ消耗硫酸少、途径Ⅱ不会产生污染大气的气体.
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分:
| 实验步骤 | 实验现象 |
| 将打磨过的铝片(过量)放入一定浓度的氯化铜溶液中 | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色 |
| 反应结束后分离出溶液备用 | |
| 红色固体用蒸馏水洗涤后,置于潮湿的空气中 | 一段时间后固体由红色变为绿色[视其主要成分为Cu2(OH)2CO3] |
置换反应2Al+3Cu2+=2Al3++3Cu;化合反应2Cu+O2+CO2+H2O=Cu2(OH)2CO3.
(2)工业上可用铝与软锰矿(主要成分为MnO2)反应来冶炼金属锰.MnO2在H2O2分解反应中作催化剂.若将适量MnO2加入酸化后的H2O2溶液中,MnO2溶解产生Mn2+.该反应的离子方程式是MnO2+H2O2+2H+═Mn2++O2↑+2H2O.
(3)某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾.其设计的实验过程如图所示:

①铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于c上(用以下所给仪器的编号填入,下同),取用坩埚应使用e,灼烧后的坩埚应放在b上,不能直接放在桌面上.实验所用仪器:a.蒸发皿 b.石棉网 c.泥三角 d.表面皿 e.坩埚钳 f.试管夹
②由粗制氧化铜通过两种途径制取胆矾,通过途径Ⅱ实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、加热蒸发、冷却结晶、过滤洗涤、自然干燥,与途径Ⅰ相比,途径Ⅱ有明显的两个优点是:产生等量胆矾途径Ⅱ消耗硫酸少、途径Ⅱ不会产生污染大气的气体.
15.化学家于1995年合成了一种分子式为C200H200的含有多个碳碳叁键的链烃,其分子中含有碳碳叁键数目最多可以是( )
| A. | 49 | B. | 50 | C. | 51 | D. | 无法确定 |
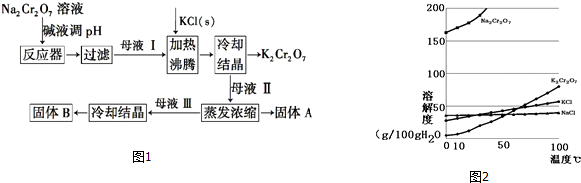

 ,甲的化学式Na2S2O4
,甲的化学式Na2S2O4