��Ŀ����
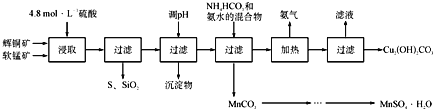
����Ŀ����ͭ����Ҫ�ɷ�Cu2S,���̿���Ҫ�ɷ�MnO2�����Ƕ���������SiO2��Fe2O3�����ʡ���ҵ���ۺ����������ֿ����Ʊ������̺ͼ�ʽ̼��ͭ����Ҫ�����������£�
��֪��
��MnO2�ܽ����������е�������Ϊ������
��[Cu(NH3)4]SO4�����ȶ�������ˮ�л�ֽ�����NH3��
��MnSO4��H2O��������ˮ�������ھƾ�;
�ܲ��ֽ�����������������ģ���ʼ������pH����������Ũ��Ϊ1.0 mol��L-1���㣺������Ũ��С��1.0��10-5ʱ����Ϊ�����ӳ�����ȫ��):
Ksp(Fe(OH)3)=1.0��10-38, Ksp(Cu(OH)2)=1.0��10-20�� Ksp(Mn(OH)2)=4.0��10-14
��1�����ʱ���õ��Ľ���Һ����Ҫ����CuSO4��MnSO4�ȡ�д���÷�Ӧ�Ļ�ѧ����ʽ_________________________________��
��2����pH�ķ�ΧΪ____________��
��3���ڸù����п�ѭ��ʹ�õ�������______________�������������� ���ڣ��¶Ȳ��ܹ���Ҳ���ܹ��ߵ�ԭ��Ϊ___��
��4�����������ͼʾ��������̼���̾�һϵ�в������MnSO4��H2O���壬���ⶨ���ȡ���ʵ�鷽������������
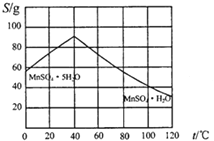
�ٽ�̼���̹�������ϡ��������������Һ;
�ڼ�����Һ�������¶�>40�棬_________�õ��ֲ�Ʒ��
��_______�����¸���ɵõ��ϴ����塣
�����ⶨ��Ʒ��Ĵ��ȣ�ȡ14.00g���������ˮ���100mL��Һ����ȡ25.00mL,��������BaCl2��Һ���õ�����4.66g�������Ʒ�Ĵ���Ϊ___(������λ��Ч����)��ijС����㷢�ֱ�����Ʒ���ȴ���100%(�ⶨ�����в��������ɺ���)�������ԭ����__(��дһ��)��
���𰸡� Cu2S+2MnO2+4H2SO4=2CuSO4+2MnSO4+S��+4H2O 3<pH<4 NH3 �¶ȹ��ͣ�[Cu(NH3)4]SO4�ֽⲻ��ȫ���¶ȹ��ߣ��ᵼ��Cu2(OH)2CO3�ֽ⣬�������������ʹ��ʽ̼��ͭ�������� �����ᾧ�����ȹ��� �þƾ�ϴ�Ӳ�Ʒ2-3�� 96.57% �����л���������(��Է�������С��MnSO4)���ʻ־���ʧȥ�ᾧˮ��
����������1�����������Ϣ��MnO2�ܽ����������е�������Ϊ������Cu2S��MnO2�������Ϻ���������ͭ�����������������ˮ����Ӧ�Ļ�ѧ����ʽCu2S+2MnO2+4H2SO4=2CuSO4+2MnSO4+S��+4H2O����ȷ���� Cu2S+2MnO2+4H2SO4=2CuSO4+2MnSO4+S��+4H2O��
��2������pH��������ʹFe3+ת��ΪFe(OH)3��������ȥ��Ksp(Fe(OH)3)=1.0��10-38,��c(Fe3+)=1.0��10-5 mol��L-1, c��OH-��=10-11 mol��L-1��c��H+��=10-3 mol��L-1��pH=3�����ǵ���ʽ̼��ͭ������Ӧ�ñ���ͭ����ʧ��Ksp(Cu(OH)2)=1.0��10-20����c(Cu2+)=1.0 mol��L-1��c��OH-��=10-10�� c��H+��=10-4 mol��L-1��pH=4�����Ե�pH�ķ�ΧΪ3<pH<4����ȷ�𰸣�3<pH<4��
��3��������������Ͷ�뷴Ӧ��Ͳ�����ﰱ����������ˮ���γɰ�ˮ��Ͷ��ѭ��ʹ�ã��ʿ�ѭ��ʹ�õ�����Ϊ������ ������������ ���ڣ��¶Ȳ��ܹ���Ҳ���ܹ��ߵ�ԭ���¶ȹ��ͣ�[Cu(NH3)4]SO4�ֽⲻ��ȫ���¶ȹ��ߣ��ᵼ��Cu2(OH)2CO3�ֽ⣬�������������ʹ��ʽ̼��ͭ�������٣���ȷ�𰸣��������¶ȹ��ͣ�[Cu(NH3)4]SO4�ֽⲻ��ȫ���¶ȹ��ߣ��ᵼ��Cu2(OH)2CO3�ֽ⣬�������������ʹ��ʽ̼��ͭ�������١�
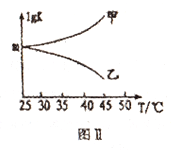
(4)��������ͼ֪���¶ȵ���40��ʱ����MnSO4��5H2O���壬����40��ʱ����MnSO4��5H2O���壬�����������Һ�Ʊ�MnSO4��5H2O��ʵ����뱣֤��Һ�¶ȸ���40�棻Ȼ��ͨ�������ᾧ�����ȹ������õ��ֲ�Ʒ����ȷ��: �����ᾧ�����ȹ�����
��Ϊ���ٲ�Ʒ����ʧ���þƾ�ϴ�Ӳ�Ʒ2-3�������¸���ɵõ��ϴ���������ȷ�����þƾ�ϴ�Ӳ�Ʒ2-3����
�����ᱵ����Ϊ4.66/233=0.02mol����������ӵ�����Ϊ0.02mol��ԭ�����к��е���������ӵ�����Ϊ0.02��100/25=0.08mol�������̾��������Ϊ0.08��169g�� �����Ʒ�Ĵ���Ϊ0.08��169/14��100%=96.57% ���ñ��Ȼ�����Һ�ⶨ��Ʒ��MnSO4��5H2O��������ʱ��������Ʒ���ȴ���100%��˵����Ʒ�����������������������MnSO4��5H2O�����������������������ֻҪ��������Ʒ���������������������ԭ��������������ԭ������Ʒ�л������������ʻ־���ʧȥ�ᾧˮ����ȷ����96.57% �������л���������(��Է�������С��MnSO4)���ʻ־���ʧȥ�ᾧˮ��

����Ŀ����ij��Br-��ˮ����ȡBr2�Ĺ��̰��������ˡ���������ȡ����ѡ�������ȡ����������Ȳ��衣
��֪����2NaOH+Cl2==NaCl+NaClO+H2O
��Br2�����������Ȼ�̼����ʮ����
���� | Br2 | CCl4 | ��ʮ���� |
�ܶ�/g��cm-3 | 3.119 | 1.595 | 0.753 |
�е㣯�� | 58.76 | 76.8 | 215��217 |
��ˮ���ܽ��� | �� | ���� | ���� |

����˵������ȷ����
A. ��װ����Br-�����ķ�ӦΪ��2Br-+Cl2===Br2+2Cl-
B. ��װ����NaOH��Һÿ����1��Cl2��ת��1��e-
C. ����װ�ý�����ȡ���ܽ�Br2���л������²�
D. �ñ�װ�ý����������ռ�������Br2