题目内容
(9分)在一个容积为500mL的密闭容器中,充入5mol H2和2 mol CO。在一定温度和一定压强下,发生如下反应在:2H2(g) +CO(g) CH3OH(g),经过5min后达到平衡状态。若此时测得容器内压强是起始时的4/7,求:(1)以H2的浓度变化表示的该反应的速率(2)达平衡时CO的转化率(3)该温度下的平衡常数K
CH3OH(g),经过5min后达到平衡状态。若此时测得容器内压强是起始时的4/7,求:(1)以H2的浓度变化表示的该反应的速率(2)达平衡时CO的转化率(3)该温度下的平衡常数K
 CH3OH(g),经过5min后达到平衡状态。若此时测得容器内压强是起始时的4/7,求:(1)以H2的浓度变化表示的该反应的速率(2)达平衡时CO的转化率(3)该温度下的平衡常数K
CH3OH(g),经过5min后达到平衡状态。若此时测得容器内压强是起始时的4/7,求:(1)以H2的浓度变化表示的该反应的速率(2)达平衡时CO的转化率(3)该温度下的平衡常数K(1) (H2) =1.2mol/(L·min)
(H2) =1.2mol/(L·min)
(2)α(CO)=C反应(CO)/ C起始(CO)×100%=75%
(3)K= C(CH3OH )/ C(CO)·C2(H2)="0.1875" (mol/(L)-2
 (H2) =1.2mol/(L·min)
(H2) =1.2mol/(L·min) (2)α(CO)=C反应(CO)/ C起始(CO)×100%=75%
(3)K= C(CH3OH )/ C(CO)·C2(H2)="0.1875" (mol/(L)-2
2H2(g) +CO(g) CH3OH(g)
CH3OH(g)
n0 5 2 0
△n 2x x x
n(平衡) 5-2x 2-x x
利用PV=nRT,在恒温、恒容下,则n0/ n(平衡)=P0/P(平衡),
(5+2)/[(5-2x)+(2-x)+x]= P0/[4/7 P0],得:x=1.5 mol
(1)υ(H2)=(2x/0.5L)/5min=1.2 mol/(L·min)
(2)CO的转化率=x/2=75%
K=3/(42×1)=0.1875(mol/(L)-2
 CH3OH(g)
CH3OH(g)n0 5 2 0
△n 2x x x
n(平衡) 5-2x 2-x x
利用PV=nRT,在恒温、恒容下,则n0/ n(平衡)=P0/P(平衡),
(5+2)/[(5-2x)+(2-x)+x]= P0/[4/7 P0],得:x=1.5 mol
(1)υ(H2)=(2x/0.5L)/5min=1.2 mol/(L·min)
(2)CO的转化率=x/2=75%
K=3/(42×1)=0.1875(mol/(L)-2

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
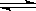 2C(g)+2D(g),
2C(g)+2D(g), 2 SO3反应。几分钟后反应达到化学平衡状态,测得容器中气体压强变为原来的90% ,则该反应达到平衡时SO2的转化率为______________。
2 SO3反应。几分钟后反应达到化学平衡状态,测得容器中气体压强变为原来的90% ,则该反应达到平衡时SO2的转化率为______________。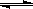 C(g)+3D(g)。现分别从两条途径建立平衡:Ⅰ—从正反应开始,A、B的起始物质的量均为2mol;Ⅱ—从逆反应开始,C、D的起始物质的量分别为2mol和6mol。以下叙述中正确的是
C(g)+3D(g)。现分别从两条途径建立平衡:Ⅰ—从正反应开始,A、B的起始物质的量均为2mol;Ⅱ—从逆反应开始,C、D的起始物质的量分别为2mol和6mol。以下叙述中正确的是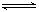 2Z,达到平衡后,X的转化率不可能为( )
2Z,达到平衡后,X的转化率不可能为( ) 2 NH3 (每生成2 mol NH3放出92.4 kJ的热量),在恒温、恒压的密闭容器中进行如下实验:①通入1 mol N2和3 mol H2,达平衡时放出热量为Q1,②通入2 mol N2和6 mol H2,达平衡时放出热量为Q2,则下列关系正确的是 ( )
2 NH3 (每生成2 mol NH3放出92.4 kJ的热量),在恒温、恒压的密闭容器中进行如下实验:①通入1 mol N2和3 mol H2,达平衡时放出热量为Q1,②通入2 mol N2和6 mol H2,达平衡时放出热量为Q2,则下列关系正确的是 ( ) 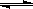 2HNO3+NO中加入O2,则化学平衡
2HNO3+NO中加入O2,则化学平衡 cZ(g), 在不同的温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间(t)的关系如图所示。下列判断不正确的是
cZ(g), 在不同的温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间(t)的关系如图所示。下列判断不正确的是