题目内容
【题目】【2017届福建省厦门大学附中高三上学期第二次月考】如图所示甲、乙是电化学实验装置。

(1) 若甲、乙两烧杯中均盛有NaCl溶液。
① 甲中石墨棒上的电极反应式为______________________________;
② 乙中总反应的离子方程式为________________________________;
③ 将湿润的淀粉KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为________________________
(2) 若甲、乙两烧杯中均盛有CuSO4溶液。
① 甲中铁棒上的电极反应式为___________________________;
② 如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25 ℃),一段时间后溶液的H变为1,若要使溶液恢复到电解前的状态,可向溶液中加入__________(填写物质的化学式)________g。
【答案】(1)①2H2O+O2+4e-═4OH-
②2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
③5Cl2+I2+6H2O═10HCl+2HIO3
(2)①Fe-2e-═Fe2+
②CuO(或CuCO3);0.8(或1.24)
【解析】
试题分析:(1) 若甲、乙两烧杯中均盛有NaCl溶液。① 甲为铁的吸氧腐蚀,石墨是正极,石墨棒上的电极反应式为2H2O+O2+4e-═4OH-;② 根据电子流向,石墨是阳极,乙为用惰性电极电解氯化钠溶液,乙中总反应的离子方程式为2Cl-+2H2O ![]() H2↑+Cl2↑+2OH-;③若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,根据电子守恒,5mol氯气失电子10mol,2mol I2得电子10mol,碘的化合价升高为+5价,该反应的化学方程式为5Cl2+I2+6H2O═10HCl+2HIO3;(2) 若甲、乙两烧杯中均盛有CuSO4溶液。① 甲为原电池,铁为负极,铁棒上的电极反应式为Fe-2e-═Fe2+;②由2CuSO4+2H2O
H2↑+Cl2↑+2OH-;③若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,根据电子守恒,5mol氯气失电子10mol,2mol I2得电子10mol,碘的化合价升高为+5价,该反应的化学方程式为5Cl2+I2+6H2O═10HCl+2HIO3;(2) 若甲、乙两烧杯中均盛有CuSO4溶液。① 甲为原电池,铁为负极,铁棒上的电极反应式为Fe-2e-═Fe2+;②由2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4,要使溶液恢复原状态,可加入CuO(或CuCO3),一段时间后溶液的pH变为1,则c(H+)=0.1mol/L,n(H+)=0.2L×0.1mol/L=0.02mol,则由电解反应可知析出的Cu的物质的量为0.01mol,由Cu原子守恒可知,m(CuO)=0.01mol×80g/mol=0.8g,或m(CuCO3)=0.01mol×124g/mol=1.24g。
2Cu+O2↑+2H2SO4,要使溶液恢复原状态,可加入CuO(或CuCO3),一段时间后溶液的pH变为1,则c(H+)=0.1mol/L,n(H+)=0.2L×0.1mol/L=0.02mol,则由电解反应可知析出的Cu的物质的量为0.01mol,由Cu原子守恒可知,m(CuO)=0.01mol×80g/mol=0.8g,或m(CuCO3)=0.01mol×124g/mol=1.24g。

 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案【题目】保护环境已成为当前和未来的一项全球性重大课题.为解决目前燃料使用过程中的环境污染问题,并缓解能源危机,有的专家提出利用太阳能促使燃料循环使用的构想,如图所示:
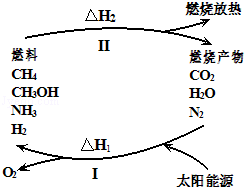
过程I可用如下反应表示:
①2CO2![]() 2CO+O2
2CO+O2
②2H2O![]() 2H2+O2
2H2+O2
③2N2+6H2O![]() 4NH3+3O2
4NH3+3O2
④2CO2+4H2O![]() 2CH3OH+3O2
2CH3OH+3O2
⑤2CO+H2O![]() +3O2
+3O2
请回答下列问题:
(1)过程I的能量转化形式为: 能转化为 能.
(2)请完成第⑤个反应的化学方程式
(3)上述转化过程中,△H1和△H2的关系是
(4)断裂1mol化学键所需的能量见表:
共价键 | H﹣N | H﹣O | N≡N | O=O |
断裂1mol化学键所需能量/kJmol﹣1 | 393 | 460 | 941 | 499 |
常温下,N2和H2O反应生成NH3的热化学方程式为

