题目内容
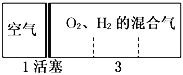
【题目】硼化钒(VB2)-空气电池是目前储电能力最高的电池,电池示意图如下,该电池工作时反应为:4VB2+11O2=4B2O3 +2V2O5。下列说法不正确的是

A. 电极a 为电池正极
B. 图中选择性透过膜为阴离子透过性膜
C. 电池工作过程中,电极a附近区域pH减小
D. VB2极发生的电极反应为:2VB2 +22OH--22e- = V2O5+2B2O3 + 11H2O
【答案】C
【解析】A、电极a通入空气,则电极a为正极,故A说法正确;B、电极a的反应式为:O2+2H2O+4e-=4OH-,负极反应式为:2VB2 +22OH--22e- = V2O5+2B2O3 + 11H2O,OH-需要向负极移动,因此选择性透过膜为阴离子透过性膜,故B说法正确;C、根据B选项分析,电极a产生OH-,pH增大,故C说法错误;D、根据电池总反应,负极反应式为2VB2 +22OH--22e- = V2O5+2B2O3 + 11H2O,故D说法正确。

练习册系列答案
相关题目